Česká a slovenská psychiatrie

Časopis
Psychiatrické společnosti ČLS JEP
a Psychiatrickej spoločnosti SLS
souborný článek / review article
MOLEKULÁRNÍ PODSTATA VZNIKU NEŽÁDOUCÍCH ÚČINKŮ HALOPERIDOLU
MOLECULAR MECHANISMS OF ADVERSE SIDE EFFECTS OF HALOPERIDOL
Martina Raudenská1, Jaromír Gumulec1, Markéta Sztalmachová1, Marie Nováková2, René Kizek3, Michal Masařík1
1 Ústav patologické fyziologie, Lékařská fakulta Masarykovy univerzity Brno
2 Fyziologický ústav, Lékařská fakulta Masarykovy univerzity Brno
3 Ústav chemie a biochemie, Mendelova univerzita Brno
2 Fyziologický ústav, Lékařská fakulta Masarykovy univerzity Brno
3 Ústav chemie a biochemie, Mendelova univerzita Brno
SOUHRN
Raudenská M, Gumulec J, Sztalmachová M, Nováková M, Kizek R, Masařík M. Molekulární podstata vzniku nežádoucích účinků haloperidolu
Haloperidol (HP) je látka ze skupiny incizivních antipsychotik (dříve označovaných neuroleptika). Je užíván k symptomatické léčbě schizofrenních, schizoafektivních a afektivních psychóz, k potlačení neklidu, agitovanosti a agresivity. Při dlouhodobém užívání se u pacientů objevovaly závažné vedlejší účinky. Jednalo se zejména o těžké postižení extrapyramidových nervových drah a následné poruchy mobility pacientů, tardivní dyskinezi (TD), prodloužení QT intervalu, výskyt arytmií a náhlé srdeční smrti. Bylo zjištěno, že v incidenci extrapyramidových poruch existují výrazné interindividuální rozdíly. Možným mechanismem cytotoxicity HP je působení oxidativního stresu. U pacientů s extrapyramidovými příznaky někdy dochází k vymizení příznaků po podání vitaminu E a jiných v tucích rozpustných antioxidantů, což je v souladu s teorií, že za vedlejší účinky HP je zodpovědná zejména peroxidace membránových lipidů. HP je antagonista dopaminu a jeho hlavním místem účinku je dopaminový receptor D2 (DRD2). HP nemá vliv pouze na signalizaci pomocí tohoto receptoru, ale ovlivňuje také jeho expresi a rovněž expresi dalších genů.
Klíčová slova: haloperidol, oxidační stres, kardiotoxicita, antipsychotikum, molekulární mechanismy
SUMMARY
Raudenská M, Gumulec J, Sztalmachová M, Nováková M, Kizek R, Masařík M. Molecular mechanisms of adverse side effects of haloperidol
Haloperidol (HP) is the most potent neuroleptic agent which has been widely used not only in psychiatric patients but also in patients with other diagnoses, mainly geriatric and surgical, for the control of severe agitation, e.g. after general anaesthesia. Haloperidol was considered to be a safe drug, but unfortunately its therapeutic effects also come with severe extrapyramidal side effects, resulting in movement disorders, tardive dyskinesia, prolonging of the corrected QT interval which can cause severe arrhythmias such as Torsade de Pointes (TdP) and eventually result in sudden cardiac death. Large interindividual differences in the incidence of side effects have been demonstrated. The possible mechanism of HP cytotoxicity is an effect of oxidative stress, especially peroxidation of membrane lipids. Support for lipid peroxidative damage in patients with movement disorders comes from reports of amelioration of TD after treatment with vitamin E, or other lipid soluble antioxidants. HP is a dopamine antagonist and its major site of action is the dopamine D2 receptor (DRD2), which exhibits high affinity for the drug. It was found that HP affects not only DRD2 signalisation, but also the expression of DRD2 and other genes.
Key words: haloperidol, oxidative stress, cardiotoxicity, antipsychotic drug, molecular mechanisms
HALOPERIDOL, METABOLISMUS A VEDLEJŠÍ ÚČINKY
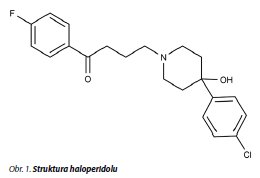
Haloperidol patří do skupiny typických incizivních antipsychotik (dříve označována jako skupina neuroleptik). Je užíván k léčbě stavů projevujících se tzv. pozitivní klinickou symptomatologií (halucinace, bludy, dezintegrace myšlení) - u schizofrenních, schizoafektivních a afektivních psychóz, k potlačení neklidu, agitovanosti a agresivity, a to nejen u psychiatrických, ale i u chirurgických a zvláště geriatrických pacientů.1,2 Poprvé byl syntetizován v roce 1956, na trhu se objevil v roce 1960 a pro svou relativně dobrou snášenlivost, široké spektrum lékových forem, nízkou cenu a celou řadu dalších vlastností se stal jedním z nejšíře užívaných antipsychotik Haloperidol náleží mezi butyrofenony (obr. 1). Je metabolizován systémem cytochromu P450 v játrech,3 s přednostním využitím izoenzymu CYP 3A4.4 Průměrný poločas eliminace HP z organismu pro 0,125 mg/kg HP podaného nitrožilně je 17,9 ?6,4 hodiny.5
Hlavním mechanismem účinku HP a jiných typických antipsychotik je blokáda dopaminových receptorů D2 (DRD2), které mají pro HP vysokou afinitu.
Jako většina typických antipsychotik má i HP závažné vedlejší účinky, jako je těžké postižení extrapyramidových nervových drah a následné poruchy mobility pacientů nebo tardivní dyskineze.6 HP totiž vedle svého terapeutického antidopaminergního působení na mezolimbický a mezokortikální systém účinkuje i v jiných lokalizacích.
Extrapyramidové nežádoucí účinky jsou zapříčiněny působením HP v buňkách nigrostriatálního systému. Shivkumar et al. pozorovali, že zvyšující se dávky HP zvyšovaly poškození extrapyramidových drah u potkaních modelů.6 Jako vedlejší účinek léčby HP bylo pozorováno rovněž zvýšení senzitivity dopaminového receptorů a tardivní dyskineze, která přetrvává i po vysazení HP.7
Bylo též zjištěno, že HP prodlužuje korigovaný QT interval, a zvyšuje tak pravděpodobnost výskytu arytmií typu Torsade de Pointes,8 které mohou vyústit až v náhlou srdeční smrt. Prodloužení QT intervalu a arytmie se objevovaly po podání běžných dávek léku orálně9 či nitrožilně,10 ale též jako důsledek předávkování HP.11 Blom et al. pozorovali, že QT se v průběhu léčby haloperidolem mění dle předchozí anamnézy. U pacientů, kteří měli před léčbou QT normální, se QT prodlužovalo, ale u pacientů s prodlouženým QT se po podání HP QT naopak zkracovalo. Jako dalším rizikovým faktorem pro prodloužení QT se ukázalo být podstoupení rozsáhlejšího chirurgického zákroku před započetím léčby HP.12 Na buněčné úrovni HP vyvolává spíše nekrózu než apoptotickou smrt buňky.3
HALOPERIDOL A INTERINDIVIDUÁLNÍ VARIABILITA
Léky a jiná xenobiotika jsou metabolizována množstvím enzymů, jejichž aktivita se liší mezi jednotlivci, etniky i rasami.14 Byly pozorovány mezirasové rozdíly v dávkách, které jsou schopny vyvolat nežádoucí účinky neuroleptik. Binder a Levy pozorovali, že narušení extrapyramidových drah dva týdny od zahájení léčby neuroleptiky se vyskytovalo u 95 % Asiatů, 67 % bělochů, ale pouze u 60 % Afroameričanů.15 Jann et al. potvrdili, že Číňané jsou při léčbě HP náchylnější k defektům extrapyramidových drah. Asiaté měli také signifikantně vyšší koncentrace HP v séru ve srovnání s bílými Američany po podání stejné dávky léku16 a schizofrenici asijského původu odpovídali lépe na léčbu nižšími dávkami HP.17
VOLNÉ KYSLÍKOVÉ RADIKÁLY AOXIDATIVNÍ STRES
Možným mechanismem cytotoxicity HP je působení oxidativního stresu. Volné kyslíkové radikály jsou velmi reaktivní entity s nespárovaným elektronem ve vnějším orbitalu. Kyslíkové radikály (ROS - Reactive Oxygen Species) zahrnují superoxidové anionty hydroxylové radikály hydrogenperoxidy singletový kyslík a další formy. Jsou produkovány hlavně v důsledku aerobní respirace,18 ale vznikají též při ?-oxidaci mastných kyselin, metabolizaci xenobiotik pomocí cytochromu P450, při redoxním cyklování chinonů, stimulaci fagocytů a metabolismu dopaminu. ROS mohou poškozovat proteiny lipidy buněčné membrány a DNA.
Za fyziologických podmínek chrání organismus před negativním působením volných radikálů komplexní systém antioxidačních enzymů. Mezi nejúčinnější antioxidační enzymy patří superoxiddismutáza (SOD), kataláza (CAT) a glutathion peroxidáza (GSHPx). Základní mechanismy antioxidačního systému jsou zachyceny na obr. 2. Rovnováha mezi ROS a antioxidační ochranou buňky je pro správné fungování buněk zcela zásadní. Vychýlení ve prospěch ROS uvádí buňky do oxidativního stresu a ten pak přímo působí nekrotickou nebo apoptotickou smrt buněk.19,20
Oxidativní stres se může v organismu projevovat mnoha způsoby. K nejzásadnějším manifestacím oxidativního stresu patří peroxidace lipidů a zvýšená produkce antioxidačních enzymů, indukce transkripčních faktorů, jako je NFkB, a aktivace proteinkináz aktivovaných mitogeny (MAPK).
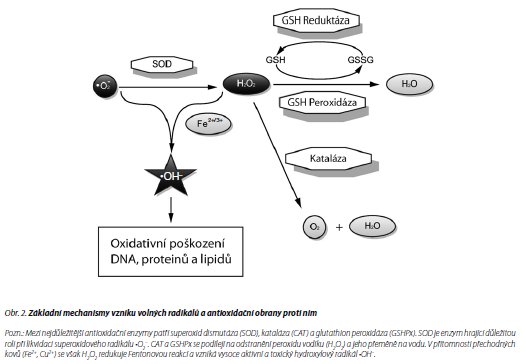
Peroxidace lipidů a zvýšená produkce antioxidačních enzymů
Zvýšená produkce superoxiddismutázy (SOD) a katalázy (CAT) se objevuje ihned po vystavení organismu ROS.21 Zvýšená produkce těchto enzymů je však pro organismus velmi zatěžující a při chronickém vystavení organismu ROS se produkce enzymů může postupně snižovat.22
Indukce transkripčních faktorů
NF?B (jaderný faktor kappa B) je protein, který se váže na regulační sekvence mnoha genů imunitního systému a účastní se regulace zánětlivých odpovědí.23 NF?B je v buňkách aktivován řadou způsobů, jedním z nich je právě oxidativní stres, zejména pak zvýšená hladina hydrogenperoxidů.20 NF?B je rovněž aktivován signály z nekrotických buněk24 Zvýšená aktivita NF?B může být blokována antioxidanty.25
Aktivace MAP kináz
Proteinkinázy aktivované mitogeny (MAPKs) jsou serin/threoninové kinázy které jsou klíčové v přenosu signálu v rámci četných signálních drah v buňce. Běžně jsou stimulovány růstovými a diferenciačními faktory.
Oxidativní stres jako možný mechanismus cytotoxicity haloperidolu
Behl et al. prokázali, že buňky odolné vůči oxidativnímu stresu jsou odolné i vůči toxickým účinkům HP,13 což implikuje roli volných radikálů v cytotoxicitě HP. Dlouhodobá léčba pomocí HP vyvolává vyšší fluktuaci dopaminu a tím zřejmě zvyšuje oxidativní zátěž organismu.6 ROS vznikají procesem oxidativní deaminace při degradaci dopaminu monoaminovou oxidázou typu B (MAO-B).6 Z těchto reaktivních metabolitů dopaminu - zejména se jedná o peroxid vodíku - může v přítomnosti katalyzátorů, jako je železo, vznikat silně neurotoxický hydroxylový radikál, který se mimo jiné podílí na peroxidaci lipidů.26 Právě díky přítomnosti železa ve své struktuře mohou volný hemoglobin a myoglobin umocňovat poškození buněk, které mají díky oxidativnímu stresu nadbytek peroxidu vodíku. Tato situace může nastat například při krvácení do mozku.26 Peroxidace lipidů působená ROS je zodpovědná za změny v synaptických signálech (snížený transport ?-aminomáselné kyseliny a dopaminu do pre-synaptických váčků).27 Přímé propojení mezi HP a vznikem peroxidů prokázali Post et al, když pozorovali akumulaci peroxidu v imortalizovaných buňkách myšího hipokampu po přidání HP do buněčné kultury. Přídavek HP ovlivňoval též intracelulární množství glutathionu (GSH). Během prvních hodin po přidání HP hladina GSH vzrostla, avšak po 16-20 hodinách nastal dramatický pokles a došlo k úbytku GSH v buňce oproti buňkám kontrolním.25 U pacientů s TD a narušenou pohyblivostí někdy dochází k vymizení příznaků po podání vitaminu E a jiných v tucích rozpustných antioxidantů, což je v souladu s teorií, že za vedlejší účinky HP je zodpovědná zejména peroxidace membránových lipidů.28 Hladiny malondialdehydů (MDA) v plazmě, které indikují narůstající oxidační stres v důsledku peroxidace membránových lipidů, byly signifikantně vyšší u pacientů léčených klasickými antipsychotiky (HP, flupentixol) ve srovnání se skupinou léčenou antipsychotiky atypickými (klozapin, amisulprid, quetiapin, risperidon, ziprasidon).29 Nejnižší hladiny MDA byly nalezeny u pacientů léčených klozapinem a amisulpridem. Olanzapin si z atypických antipsychotik vedl nejhůře a mírou peroxidace lipidů byl srovnatelný s klasickými antipsychotiky.30,31
Burkhardt et al. také zjistili, že neuroleptika, jako je HP, chlorpromazin a thiothixen, inhibují NADH-ubichinonoxidoreduktázu (komplex-I dýchacího řetězce). Ačkoli respirační řetězec je hlavním zdrojem ROS v organismu, jeho inhibice vzniku ROS spíše napomáhá.18 Inhibice komplexu-I dýchacího řetězce by tak mohla být jednou z dalších příčin ireverzibilního poškození extrapyramidových drah u pacientů léčených neuroleptiky.32
HALOPERIDOL A VLIV NA EXPRESI GENŮ
Dopaminový receptor DRD2
HP je antagonista dopaminu a hlavním místem jeho účinku je tedy dopaminový receptor. Dopaminové receptory se řadí do dvou skupin: D1 a D5 tvoří skupinu dopaminových receptorů typu D1 (D1-like receptors), D2-D4 tvoří skupinu receptorů typu D2 (D2-like receptors). Základní rozdíl mezi těmito dvěma skupinami je v jejich účinku na post-synaptický neuron. Aktivace receptorů skupiny D1 může vést k excitaci a inhibici postsynaptických neuronů, zatímco aktivace receptorů skupiny D2 vede spíše jen k inhibičním reakcím. HP se váže na receptor D2 (DRD2). Bylo zjištěno, že HP nemá vliv pouze na signalizaci DRD2 receptorů, ale ovlivňuje také expresi genu DRD2, jímž je tento receptor kódován. Dlouhodobé podávání HP zvyšovalo tvorbu DRD2 mRNA a naopak snižovalo expresi D1 a D5 subtypů dopa-minového receptorů, k nimž má HP minimální afinitu.33
Dopaminový transportér DAT1
Dopaminový transportér (DAT1) je integrální membránový protein, který je nejdůležitějším regulátorem aktivního zpětného vstřebávání dopaminu ze synaptické štěrbiny; jeho exprese je podáváním HP aktivována.34
Receptor IP3R
Působením HP dochází kzvyšování exprese receptorů pro inositol 1,4,5-trisfosfát v nervových buňkách srdečních síní, což má vliv na Ca2+ srdeční signalizaci a možný vznik prodlouženého QT intervalu.35
Kináza SGK
Ke zvýšení exprese po podání HP dochází také u SGK (kinázy regulované sérem a glukokortikoidy).36 SGK chrání synaptické glutamátové transportéry před degradací v proteazomech.36 Dále také inhibuje expresi transkripčního faktoru FOXO, který se podílí na pozitivní regulaci exprese antioxidačních enzymů SOD a katalázy a na negativní regulaci exprese cyklinu D.37
Protein EPB41L1
EPB41L1 (Erythrocyte membrane protein band 4,1-like protein 1) je protein, který stabilizuje DRD2 a DRD3 na plazmatické membráně neuronu. Jeho exprese se po podání HP zvyšuje.34
Vliv HP na expresi zmiňovaných genů je zachycen na obr. 3.
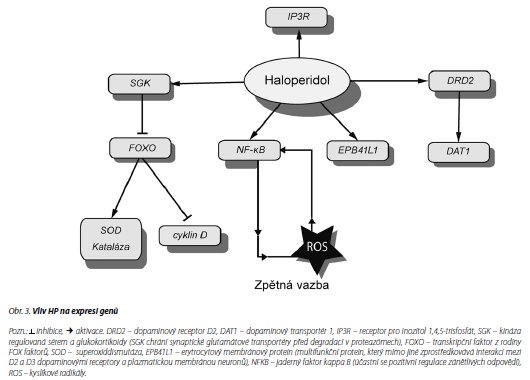
ZÁVĚR
Haloperidol (HP) byl zaveden na trh v 60. letech 20. století a záhy začal být běžně používán při léčbě mnoha psychiatrických onemocnění, zejména pak akutní a chronické schizofrenie. Známým mechanismem jeho působení je blokace dopaminového receptorů (DRD2). Mechanismy nežádoucích vedlejších účinků, zejména extrapyramidové, byly zkoumány až později. Ukázalo se, že HP a jiná klasická antipsychotika mohou vyvolávat oxidativní stres, a to mnoha cestami (zvýšený metabolismus dopaminu, úbytek GSH v buňce, indukce transkripčního faktoru NF?B, inhibice komplexu-I dýchacího řetězce). Výsledkem oxidativního stresuje peroxidace membrán a z ní vyplývající změny v synaptických signálech. Dalším mechanismem vzniku nežádoucích účinků při podávání HP je pak aktivace nebo inhibice exprese genů, jejichž produkty zasahují do buněčných procesů, jako je vedení signálu v srdečních buňkách, antioxidační bariéra, dělení buněk, zánět a další.
Na příkladu HP můžeme vidět, jak je důležité znát přesné mechanismy účinku léku, možné rozdíly v dávkování u různých etnik a pokud možno dopad podávané látky v kontextu celého organismu. Větší pozornost by též měla být věnována možnému přínosu podávání antioxidantů pro zmírnění nežádoucích účinků klasických antipsychotik.
LITERATURA
- 1. Jirák R. Organicky a symptomaticky podmíněné duševní poruchy. In: Raboch J, Zvolský P, eds. Psychiatrie. 1. vyd. Praha: Galén; 2001: 143-167.
- 2. Sulcová A, Gaier N, Doležal T et al. Látky ovlivňující centrální nervový systém. In: Lincová D, Farghali H, eds. Základní a aplikovaná farmakologie. 2. vyd. Praha: Galén; 2007: 137-218.
- 3. Igarashi K, Kasuya F, Fukui M et al. Studies on the metabolism of haloperidol (HP): the role of CYP3A in the production of the neurotoxic pyridinium metabolite HPP+ found in rat brain following ip administration of HP. Life Sci 1995; 57 (26): 2439-2446.
- 4. Fang J, Baker GB, Silverstone PH et al. Involvement of CYP3A4 and CYP2D6 in the metabolism of haloperidol. Cell Mol Neurobiol 1997; 17 (2): 227-233.
- 5. Holley FO, Magliozzi JR, Stanski DR et al. Haloperidol kinetics after oral and intravenous doses. Clin Pharmacol Ther 1983; 33 (4): 477-484.
- 6. Shivkumar BR, Ravindranath V. Oxidative stress Induced by administration of the neuroleptic drug haloperidol is attenuated by higher doses of haloperidol. Brain Res 1992; 595: 256-262.
- 7. Casey DE. Neuropsychiatry of involuntary movement disorders: tardive dyskinesia. Current Opinion in Psychiatry 1991; 4: 86-89.
- 8. Kriwisky M, Perry GY, Tarchitsky D, Gutman Y, Kishon Y. Haloperidol-induced torsades-de-pointes. Chest 1990; 98 (2): 482-484.
- 9. Fayer SA. Torsades de pointes ventricular tachyarrhythmia associated with haloperidol. J Clin Psychopharmacol 1986; 6: 375-376.
- 10. Hunt N, Stern TA. The association between intravenous haloperidol and Torsades de Pointes. Three cases and a literature review. Psychosomatics 1995; 36: 541-549.
- 11. Henderson RA, Lane S, Henry JA. Life-threatening ventricular arrhythmia (torsades de pointes) after haloperidol overdose. Hum Exp Toxicol 1991; 10: 59-62.
- 12. Blom MT, Bardai A, van Munster BC et al. Differential Changes in QTc Duration during In-Hospital Haloperidol Use. PLoS ONE 2011; 6 (9): 1.
- 13. Behl C, Lezoulac'h F, Widmann M et al. Oxidative stress-resistant cells are protected against haloperidol toxicity. Brain Res 1996; 717 (12): 193-195.
- 14. Lin KM. Psychopharmacology in cross-cultural psychiatry. Mount Sinai Journal of Medicine 1996; 63: 283-284.
- 15. Binder E, Levy R. Extrapyramidal reactions in Asians. American Journal of Psychiatry 1981; 138: 1243-1244.
- 16. Jann M, Chang W, Davis C et al. Haloperidol and reduced haloperidol plasma levels in Chinese vs non Chinese psychiatric patients. Psychiatry Research 1989; 30: 45-52.
- 17. Lin KM, Poland RE, Nuccio I et al. A longitudinal assessment of haloperidol doses and serum concentrations in asian and Caucasian schizophrenic-patients. American Journal of Psychiatry 1989; 146 (10): 1307-1311.
- 18. Hodnick WF, Duval DL, Pardini RS. Inhibition of mitochondrial respiration and cyanide-stimulated generation of reactive oxygen species by selected flavonoids. Biochem Pharmacol 1994; 47 (3): 573-580.
- 19. Mark RJ, Hensley K, Butterfield DA, Mattson MR Amyloid beta-peptide impairs ion-motive ATPase activities: evidence for a role in loss of neuronal Ca2+ homeostasis and cell death. J Neurosci 1995; 15 (9): 6239-6249.
- 20. O'Neill LA, Kaltschmidt C. NF-kappa B: a crucial transcription factor for glial and neuronal cell function. Trends Neurosci 1997; 20 (6): 252-258.
- 21. Lawler JM, Powers SK. Oxidative stress, antioxidant status, and the contracting diaphragm. Can J Appl Physiol 1998; 23(1): 23-55.
- 22. Vaziri ND, Dicus M, Ho ND et al. Oxidative stress and dysregulation of superoxide dismutase and NADPH oxidase in renal insufficiency Kidney Int 2003; 63(1): 179-185.
- 23. Baeuerle PA, Henkel T. Function and activation of NF-kappa B in the immune system. Annu Rev Immunol 1994; 12.
- 24. Li Y, Zhang W, Mantell LL et al. Nuclear factor-kappa B is activated by hyperoxia but does not protect from cell death. J Biol Chem 1997; 272 (33): 20646-20649.
- 25. Post A, Holsboer F, Behl C. Induction of NF-kappaB activity during haloperidol induced oxidative toxicity in clonal hippocampal cells: suppression of NFkappaB and neuroprotection by antioxidants. J Neurosci 1998; 18 (20): 8236-8246.
- 26. Halliwell B. Reactive oxygen species and the central nervous system. J Neurochem 1992; 59: 1609-1623.
- 27. Rafalowska U, Liu GJ, Floyd RA. Peroxidation induced changes in synaptosomal transport of dopamine and ?-aminobutyric acid, free radic biol med 1989; 6 (5): 485-92.
- 28. Egan MF, Hyde, T.M., Albers, G.W et al. Treatment of tardive dyskinezia with vitamin E. Am J Psychiatry 1992; 149: 773-777.
- 29. Dobrin I, Ciobica A, Padurariu M et al. Comparison between the effects of typical and atypical antipsychotics on oxidative stress status in schizophrenic patients 2010.
- 30. Kropp S, Kern V, Lange K et al. Oxidative stress during treatment with first- and second-generation antipsychotics. J Neuropsychiatr Clin Neurosci 2005; 17 (2): 227-231.
- 31. Park SW, Lee CH, Lee JG et al. Protective effects, of atypical antipsychotic drugs against MPP+-induced oxidative stress in PC12 cells. Neurosci Res 2011; 69 (4): 283-290.
- 32. Burkhardt C, Kelly JP, Lim YH et al. Neuroleptic medications inhibit complex I of the electron transport chain. Ann Neurol 1993; 33 (5): 512-517.
- 33. Lidow MS, GoldmanRakic PS. Differential regulation of D-2 and D-4 dopamine receptor mRNAs in the primate cerebral cortex vs. neostriatum: Effects of chronic treatment with typical and atypical antipsychotic drugs. Journal of Pharmacology and Experimental Therapeutics 1997; 283 (2): 939-946.
- 34. Moran LB, Graeber MB. Towards a pathway definition of Parkinsons disease: a complex disorder with links to cancer, diabetes and inflammation. Neurogenetics 2008; 9 (1): 1-13.
- 35. Novákova M, Sedlákova B, Sirova M, Fialová K, Krizanova O. Haloperidol increases expression of the inositol 1,4,5-trisphosphate receptors in rat cardiac atria, but not in ventricles. General Physiology and Biophysics 2010; 29 (4): 381-389.
- 36. James AB, Conway AM, Morris BJ. Regulation of the neuronal proteasome by Zif268 (Egrl). Journal of Neuroscience 2006; 26 (5): 1624-1634.
- 37. Coffer PJ, Burgering BMT Forkhead-box transcription factors and their role in the immune system. Nature Reviews Immunology 2004; 4 (11): 889-899.





