Česká a slovenská psychiatrie

Časopis
Psychiatrické společnosti ČLS JEP
a Psychiatrickej spoločnosti SLS
souborný článek / review article
COVID-19 V TEHOTENSTVE - RIZIKOVÝ FAKTOR VZNIKU PORÚCH AUTISTICKÉHO A SCHIZOFRENICKÉHO SPEKTRA U POTOMKOV?
COVID-19 IN PREGNANCY - A RISK FACTOR FOR AUTISTIC AND SCHIZOPHRENIC SPECTRUM DISORDERS IN THE OFFSPRING?
Ivan Belica1,2, Ivan Szadvári1, Katarína Babinská1
1 Fyziologický ústav LF UK, Bratislava, Slovenská republika
2 Výskumný ústav detskej psychológie a patopsychológie, Bratislava, Slovenská republika
2 Výskumný ústav detskej psychológie a patopsychológie, Bratislava, Slovenská republika
Práca bola podporená grantmi APVV-20-0139, APVV-20-0070.
SÚHRN
Belica I, Szadvári I, Babinská K. COVID-19 v tehotenstve - rizikový faktor vzniku porúch autistického a schizofrenického spektra u potomkov?
Porucha autistického spektra (PAS) a schizofrénia majú genetický základ, ale významnú úlohu v etiopatogenéze zohrávajú aj faktory prostredia. Jedným z nich môže byť infekčné ochorenie, ktoré matka prekoná počas tehotenstva. Vyplýva to predovšetkým z epidemiologických štúdií, podľa ktorých prenatálna infekcia za určitých okolností zvyšuje riziko vzniku PAS a schizofrénie u potomkov. Animálne experimenty naznačujú, že kľúčovú úlohu tu zohráva najmä imunitná odpoveď matky na infekciu, predovšetkým v podobe cytokínovej búrky. Výsledný efekt prenatálnej infekcie však závisí od viacerých rizikových a protektívnych faktorov na strane matky i plodu, ako aj od charakteristík pôsobiacej infekcie. V prípade COVID-19 zatiaľ pre krátkosť času takéto štúdie absentujú, no vzhľadom na jeho infekčný charakter a najmä vysoký výskyt nie je neopodstatnené uvažovať o možnom riziku. Cieľom našej práce bolo zosumarizovať výsledky epidemiologických a animálnych štúdií súvisiacich s inými infekciami a na ich základe uvažovať, či COVID-19 počas tehotenstva môže predstavovať riziko pre vznik PAS alebo schizofrénie u potomkov.
Klíčová slova: autizmus, COVID-19, cytokíny, gravidita, schizofrénia
SUMMARY
Belica I, Szadvári I, Babinská K. COVID-19 in pregnancy - a risk factor for autistic and schizophrenic spectrum disorders in the offspring?
Autism spectrum disorder (ASD) and schizophrenia have a genetic basis, but environmental factors also play a significant role in their etiopathogenesis. One of them may be an infectious disease in the mother during pregnancy. This is indicated mainly by the epidemiological studies, in which a prenatal infection has been shown to increase under certain circumstances the risk of ASD and schizophrenia in the offspring. Animal experiments indicate that the immune response of the mother plays a key role here, especially in the form of a cytokine storm. However, the resulting effect of the prenatal infection depends on several risk and protective factors on the side of the mother and the fetus, as well as on the characteristics of the infections. In case of COVID-19, due to the shortness of time, such studies are absent, however, due to its infectious nature, and predominantly its high prevalence rates, it is reasonable to consider this disease as a potential risk. The objective of our paper was to summarize results of epidemiological and animal studies in respect to other infections and, based on that, to analyse whether COVID-19 during pregnancy represents a risk for the development of ASD or schizophrenia in the offspring.
Key words: autism, COVID-19, cytokines, pregnancy, schizophrenia
ÚVOD
Kým poruchy autistického spektra (PAS) sú preukázateľne poruchou vývinu nervového systému, neurovývinová povaha schizofrénie je zatiaľ predmetom diskusií.1 Hoci obe ochorenia majú genetický základ, významným etiopatogenetickým faktorom sú aj vplyvy prostredia. Jedným z diskutovaných faktorov je prekonanie infekčného ochorenia matky počas tehotenstva. V texte predkladáme výsledky epidemiologických štúdií, ktoré uvedenú spojitosť naznačujú. Hoci prenatálna infekcia zvyšuje riziko vzniku PAS aj schizofrénie, ide o samostatné poruchy. Uvádzame tiež experimenty na zvieracích modeloch, ktoré približujú možné patomechanizmy pôsobenia prenatálnej infekcie na neurovývin a behaviorálne prejavy potomkov. Túto tému považujeme za obzvlášť dôležitú vzhľadom na nedávnu pandémiu koronavírusu SARS-CoV-2 a s ním spojené ochorenie COVID-19.2 Na záver preto zosumarizujeme, či COVID-19 u tehotných žien má predpoklady zvyšovať riziko vzniku porúch z okruhu autistického a schizofrenického spektra u potomkov.
PRENATÁLNA INFEKCIA A PORUCHY AUTISTICKÉHO SPEKTRA - EPIDEMIOLOGICKÉ ŠTÚDIE
Jeden z prvých náznakov, že prenatálna infekcia môže predstavovať riziko pre vznik PAS, priniesla epidémia vírusu rubeoly v roku 1964 v USA.3 Infekcia vtedy zasiahla aj veľké množstvo tehotných žien a viac ako 20 000 detí sa narodilo s kongenitálnym rubeolovým syndrómom. Psychiatrička Stella Chessová vyšetrila 243 detí v predškolskom veku, ktorých matka prekonala túto infekciu počas tehotenstva, pričom u 18 detí zistila PAS, čo predstavovalo 7,4% výskyt, teda 200-násobne vyšší ako v bežnej populácií v tom období.3 Odvtedy sa uskutočnilo viacero výskumov, ktoré sledovali súvislosť infekcie počas tehotenstva a rizika vzniku PAS u detí, pričom metaanalýza preukázala, že infekcia matky počas tehotenstva toto riziko zvyšuje.4 V skupine detí, ktorých matka mala infekciu, bol výskyt PAS vyšší o 13 % než v kontrolnej skupine. Hlbšia analýza ukázala, že riziko závisí od typu infekcie, fázy tehotenstva a lokalizácie infekcie. Vírusová infekcia nepredstavovala signifikantné riziko pre vznik PAS. Bakteriálna infekcia signifikantne zvyšovala riziko PAS ak bola prítomná počas 2. a 3. trimestra, a to o 20 % a 22 %, kým prvý trimester rizikový nebol. Pri skupine ostatných typov infekcií, ako sú parazitárne, hubové a ďalšie, riziko PAS signifikantne taktiež vzrástlo, ak boli prítomné počas 2. a 3. trimestra.4 Dôležitá bola aj lokalizácia infekcie. Spojitosť bola významná v prípade urogenitálnych infekcií (9 %), ale nie v prípade gastrointestinálnych ani respiračných infekcií. V prípade urogenitálnych infekcií však metaanalýza zahrnula len tie, ktoré boli bakteriálne, a v ostatných prípadoch boli zmiešané bakteriálne a vírusové, čo mohlo ovplyvniť výsledok analýzy. Ak si liečba infekcie vyžadovala hospitalizáciu matky, riziko výrazne vzrástlo najmä v druhom trimestri na 40 %.4 Podľa autorov u týchto žien tak pravdepodobne nastala silnejšia imunitná odpoveď ako u žien, ktorých stav si hospitalizáciu nevyžadoval. Niektoré štúdie skúmali špecificky súvislosť horúčky a PAS. V nórskej prospektívnej štúdii sa zistilo, že v skupine detí tých matiek, ktoré prekonali horúčku počas tehotenstva, bol výskyt PAS tiež vyšší o 40 %.5 Ak matka prekonala minimálne tri epizódy horúčky, predovšetkým v 2. trimestri, riziko prítomnosti PAS bolo oproti kontrolnej skupine až 3krát vyššie.5 Horúčku ako rizikový faktor vzniku PAS preukázala aj prospektívna bostonská štúdia.6 Podľa nej, horúčka, bez ohľadu na fázu tehotenstva, zvyšovala riziko vzniku PAS dvojnásobne, ale ak sa vyskytla osobitne počas 3. trimestra, zvýšila riziko vzniku PAS 2,7-násobne.
Novšia metaanalýza Tioleca et al. z roku 20217 preukázala silnejšiu asociáciu prenatálnej infekcie a rizika vzniku PAS ako metaanalýza Jianga et al. z roku 2016.4 Tioleco et al.7 zistili, že u detí matiek, ktoré mali počas gravidity infekciu, je o 32 % vyšší výskyt PAS. Pri analýze podľa typu infekcie sa ukázalo, že nielen bakteriálna, ale aj vírusová infekcia zvyšujú riziko vzniku PAS, a to veľmi podobne, približne na úrovni 24 %. Hubové infekcie a toxoplazmóza neboli signifikantne spojené s rizikom vzniku PAS. Pri zohľadnení fázy tehotenstva sa ukázalo, že najsilnejší efekt mala infekcia v druhom trimestri (26 %), najslabší a na hranici signifikancie v prvom trimestri (13 %). Podľa autorov tejto štúdie by prevencia alebo liečba prenatálnych infekcií mohli znížiť incidenciu PAS o 12-17 %. Tioleco et al.7 tak predpokladajú kauzálnu spojitosť prenatálnej infekcie a rizika PAS. Nedávna švédska štúdia priniesla na diskutovanú tému ešte iný pohľad.8 Brynge et al.8 síce preukázali, že infekcia v tehotenstve zvyšuje riziko vzniku PAS, ale zároveň preukázali, že aj infekcia matky počas posledného roka pred tehotenstvom bola spojená s rizikom vzniku PAS. Matky detí s PAS tak podľa nich majú vo všeobecnosti zvýšenú náchylnosť na infekčné ochorenia. Je možné, že tieto matky majú určité genetické varianty, ktoré na jednej strane vedú k náchylnosti na infekčné ochorenia a na druhej strane vedú k zvýšenému riziku PAS. Ako však dodávajú, to nevyhnutne nevylučuje kauzálny efekt prenatálnej infekcie na riziko vzniku PAS.
PRENATÁLNA INFEKCIA A PORUCHY SCHIZOFRENICKÉHO SPEKTRA - EPIDEMIOLOGICKÉ ŠTÚDIE
Podobne ako pri PAS, výskumy potvrdili, že vystavenie plodu určitým infekčným agens počas vývinu in utero môže viesť k zvýšenému riziku vzniku schizofrénie.9 Zistilo sa, že riziko je zvýšené pri expozícii vírusovým, bakteriálnym aj parazitárnym antigénom. Pri vírusových antigénoch sa skúmal vplyv prenatálnej infekcie vírusom chrípky na riziko vzniku schizofrénie a všeobecne psychóz. Preukázalo sa, že ak sa matka nakazí chrípkou počas prvej polovice tehotenstva, riziko vzniku schizofrénie je trikrát vyššie. Pri nákaze v prvom trimestri sa zvýšilo riziko schizofrénie až sedemnásobne. Je zaujímavé, že pri infekcii vírusom chrípky počas druhej polovice gravidity sa nepozorovalo žiadne zvýšené riziko schizofrénie.10 Iná štúdia sa zaoberala tretím trimestrom tehotenstva, kde sa ukázalo, že nákaza matky vírusom chrípky typu B (nie však typu A) je asociovaná s významnejším kognitívnym deficitom u potomkov, ktorým sa v priebehu života diagnostikovala schizofrénia v porovnaní s jedincami so schizofréniou, ktorí neboli exponovaní prenatálnej infekcii.11 Samotná prenatálna expozícia chrípke typu B v kontrolnej skupine jedincov bez psychózy k zhoršeniu kognitívnych schopností neviedla. Tieto štúdie naznačujú, že čas infikovania v rámci tehotenstva, virulencia kmeňa chrípky, ako aj miera imunitnej odpovede matky na infekciu sa pravdepodobne spolupodieľajú na patogenéze poruchy mozgu.11 Medzi ďalšie vírusové ochorenia, ktoré sa skúmali, patria choroby spôsobené vírusom herpes simplex (HSV) a cytomegalovírusom (CMV), ako aj rubeola. Pri nákaze typom HSV-1 sa zvýšené riziko schizofrénie nepotvrdilo, zatiaľ čo pri type HSV-2 sú výsledky z rôznych štúdii nekonzistentné. Najnovšie štúdie túto asociáciu skôr vyvrátili.12 Čo sa týka CMV infekcie in utero, nakazenie bolo spojené s dvojnásobne zvýšeným rizikom schizofrénie.12 Ešte silnejšie asociácie sa zistili u jedincov s vyššími hladinami protilátok proti CMV.13 Prenatálna expozícia rubeole tiež zvyšovala prevalenciu schizofrénie a iných porúch spektra schizofrénie s 10- až 15-násobným nárastom rizika.14,15 Vďaka očkovaniu bola rubeola v priemyselných krajinách prakticky eliminovaná. Napriek tomu zostáva hrozbou v mnohých rozvojových krajinách.15 Táto štúdia zdôrazňuje dôležitosť očkovania pri prevencii schizofrénie alebo iných porúch schizofrenického spektra.
Nielen vírusové ochorenia, ale aj bakteriálna infekcia, ktorú matka prekoná počas tehotenstva, môže byť spojená s významne zvýšeným rizikom vzniku schizofrénie a príbuzných psychóz medzi potomkami. Podľa štúdie, ktorú uskutočnili Lee et al.,16 lokalizovaná bakteriálna infekcia predstavovala 1, 6-násobné zvýšenie pravdepodobnosti vzniku psychotickej poruchy v dospelosti a systémová bakteriálna infekcia takmer trojnásobné zvýšenie pravdepodobnosti. Podobne ako pri PAS, aj v súvislosti so schizofréniou existuje štúdia, ktorej autori poukázali na to, že bakteriálna infekcia nemusí zvyšovať riziko len počas prenatálneho obdobia.17 Zistili, že všeobecne zvýšená familiárna náchylnosť zo strany otca i matky na bakteriálne infekcie so závažnejším priebehom (či už kvôli genetickej predispozícií, alebo horším životným podmienkam) by mohla predstavovať nezávislý rizikový faktor pre vznik schizofrénie u ich potomkov. Validita výsledkov týchto štúdií, čo sa týka vplyvu infekcie na prenatálny vývin, by mala byť preto potvrdená ďalším výskumom.
Viaceré štúdie tiež potvrdili, že infekcia matky parazitom Toxoplasma gondii (T. gondii) počas tehotenstva zvyšuje riziko vzniku psychóz. T. gondii je intracelulárny parazit, ktorý zvyčajne u ľudí nespôsobuje vážne komplikácie. Výnimkou sú imunokompromitovaní pacienti a plody, ktoré sa infikujú počas tehotenstva. Prvýkrát preukázala asociáciu medzi prenatálnou infekciou T. gondii a rizikom schizofrénie štúdia z roku 2005, kde sa zistilo, že zvýšená koncentrácia imunoglobulínu G (IgG) proti toxoplazme v krvi matky sa spája so zvýšeným rizikom schizofrénie a iných porúch schizofrenického spektra.18 K podobným výsledkom sa dopracovala dánska štúdia z roku 2007, ktorá podporuje súvislosť medzi vysokými hladinami IgG proti T. gondii (zodpovedajúce hornému kvartilu) a skorým nástupom schizofrénie vo veku 18 rokov a menej.19 Xiao et al.20 tiež zistili, že pre potomkov matiek nakazených toxoplazmou predstavovala infekcia významne zvýšené riziko vzniku psychóz v porovnaní s potomkami kontrolných matiek, ktoré infekciu neprekonali. Riziko bolo v tomto prípade obzvlášť zvýšené pre afektívne psychózy. Dánska štúdia však nezistila žiadnu významnú súvislosť medzi markermi infekcie a inými poruchami podobnými schizofrénii alebo afektívnymi poruchami.19 Rozdielnosť výsledkov týchto štúdií by mohla byť daná geografickými rozdielmi (t. j. biologickými rozdielmi medzi genotypmi toxoplazmy v rôznych regiónoch) alebo časovými rozdielmi (t. j. fázou tehotenstva, počas ktorej bola matka infekcii exponovaná).20,21
PATOMECHANIZMY PRENATÁLNEJ INFEKCIE - EXPERIMENTÁLNE ANIMÁLNE ŠTÚDIE
Keďže prenatálna infekcia matky za určitých okolností zvyšuje riziko vzniku PAS a schizofrénie, je namieste otázka, aké mechanizmy sa tu uplatňujú. Experimenty na zvieratách naznačujú, že plod väčšinou pravdepodobne nie je ovplyvnený priamo samotným infekčným agensom, ale predovšetkým imunitnou odpoveďou matky, ktorú vyvolá.22 Spomedzi imunitných mechanizmov tu zohrávajú úlohu najmä cytokíny a imunoglobulíny. Lipopolysacharid (LPS), ktorý napodobňuje prítomnosť a účinok gram-negatívnych baktérií, podaný gravidným samiciam potkana zvýšil koncentrácie určitých cytokínov v sére matky, v plodovej vode i v mozgu plodu na veľmi podobné hodnoty.23 Nárast sa zistil už po 4 hodinách, a hoci po 24 hodinách koncentrácie klesli, stále boli významne zvýšené v porovnaní s pôvodnými hladinami. Keď sa podala gravidným myšiam injekcia kyseliny polyinozinovej-polycitidilovej (poly(I:C)), ktorá napodobňuje prítomnosť a účinok dvojvláknových RNA vírusov, spôsobila nárast hladín viacerých cytokínov v mozgu plodu po 6 hodinách, pričom analýza po 24 hodinách preukázala stále signifikantne zvýšenú hladinu IL-1b.24 Tieto a ďalšie štúdie tak preukázali, že bakteriálna aj vírusová infekcia významne zvyšujú koncentrácie cytokínov v tele matky aj plodu, hoci presný vzorec cytokínovej odozvy sa môže líšiť v závislosti od živočíšneho druhu, typu podnetu, fázy gravidity a podobne. Do cytokínovej kaskády sú pravdepodobne zapojené predovšetkým TNF (tumor necrosis factor) a interleukíny IL-6, IL-1b, IL-17.25 Úlohu cytokínov podčiarkujú aj výskumy, v ktorých injikovali gravidným zvieratám cytokíny samotné, pričom dosiahli rovnaké fyziologické a behavi-orálne účinky ako po vystavení bakteriálnym a vírusovým podnetom. Keďže nie je možné vykonávať podobné experimenty na ľuďoch, je aspoň snaha zistiť, či koncentrácia cytokínov v sére tehotných žien a v plodovej vode dokáže predikovať riziko vzniku neuropsychiatrických ochorení u potomkov. Zistilo sa napríklad, že koncentrácia cytokínov IL-6, TNF, IL-1b, teda práve tých, na ktoré poukazujú zvieracie experimenty, bola významne vyššia v sére tých tehotných matiek, ktorých potomkovia mali neskôr diagnostikovanú psychózu, v porovnaní s matkami, ktorých potomkovia mali neurotypický vývin.26 Rozdiely v koncentráciách boli najvyššie v prvej polovici tehotenstva (7-20. týždeň), neskôr bol rozdiel nevýznamný. Hoci viaceré štúdie preukázali spojitosť medzi hladinou určitých cytokínov v sére matky počas tehotenstva alebo v plodovej vode a rizikom vzniku PAS a schizofrénie, výsledky väčšinou nie sú jednotné v tom, ktorý cytokínový profil je ten rizikový.
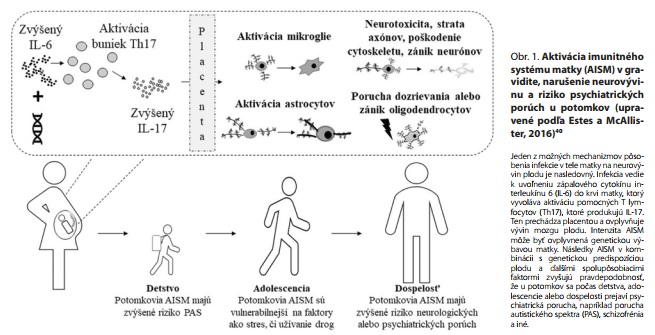
Uvažuje sa, že materské cytokíny môžu mať priamy alebo sprostredkovaný dopad na mozog plodu minimálne tromi spôsobmi alebo cestami.27 Po prvé, cytokíny z cirkulácie matky prestúpia cez placentu do krvi plodu a pôsobia priamo v mozgu. Druhá možnosť je, že cytokíny prítomné v krvi matky vyvolávajú v bunkách placenty tvorbu nových cytokínov, ktoré sa dostanú do cirkulácie plodu a následne do mozgu. Po tretie, cytokíny matky môžu prejsť cez placentu a pôsobiť na imunitný systém plodu alebo na mikrogliové bunky v mozgu plodu, ktoré aktivujú a spúšťajú v nich syntézu nových cytokínov. Bez ohľadu na to, ktorá z uvedených ciest sa uplatňuje, mozog plodu je vystavený nadmernému pôsobeniu cytokínov. Neuróny a glia exprimujú receptory pre cytokíny aj v čase, keď zápal nie je prítomný.27 Výskumy priniesli zaujímavé zistenie, že cytokíny nie sú len sprostredkovateľmi imunitnej odpovede, ale sú v mozgu syntetizované a uvoľňované aj v čase, keď organizmus nie je vystavený infektu, a sú nevyhnutné pre normálny vývin mozgu v prenatálnom období. Zúčastňujú sa na neurogenéze, migrácii neurónov, synaptogenéze či gliogenéze, čím pomáhajú budovať základ pre normálne psychické fungovanie jedinca.28 Je však potrebné, aby bunky boli vystavené ich pôsobeniu v správnom čase a v optimálnom množstve, pretože príliš nízka alebo príliš vysoká koncentrácia cytokínov v kritickom období vývinu môže zanechať negatívne dopady. Tie sa môžu prenatálne a postnatálne prejaviť na stavbe a funkcii mozgu, ako aj na behaviorálnej úrovni, v podobe rôznych neurologických alebo psychiatrických chorôb a porúch.29 Práve táto situácia môže nastať, ak je mozog plodu vystavený nadmernému pôsobeniu cytokínov pri imunitnej odpovedi matky na infekciu. Závažnosť alebo konkrétna podoba dopadu závisí od viacerých faktorov, ako je napr. fáza vývinu, v ktorej sa plod nachádza, typ infektu, infekčná nálož, ale aj od genetických či epigenetických charakteristík matky a plodu, s ktorými súvisí napr. intenzita cytokínovej odpovede.30 Zjednodušené schematické znázornenie jedného z možných mechanizmov pôsobenia infekcie na neurovývin je na obr. 1. Ďalšou otázkou je, ako cytokíny spôsobujú nežiadúce neuroanatomické a neurofyziologické zmeny. Mechanizmov je pravdepodobne viacero, no najčastejšie sa udáva krátkodobá a dlhodobá (epigenetická) zmena expresie génov.25 Animálne modely aktivácie imunitného systému matky preukázali zmenu expresie stoviek až tisícov génov. Napríklad v už spomínanej štúdii Oskviga et al.,23 kedy podávali myšiam LPS, sa v porovnaní s kontrolnou skupinou preukázala zmena expresie 3285 génov, z ktorých mnohé sa podieľajú na regulácii vývinu mozgu, napr. na dozrievaní a migrácii GABAergných interneurónov. Medzi päticu génov, u ktorých sa preukázal najväčší útlm expresie, patril aj gén AUTS2, ktorý sa v iných štúdiách ukázal ako kandidátny gén pre PAS. Výsledky štúdií sú ale zatiaľ len málo jednotné v tom, ktoré gény a akým spôsobom sú zasiahnuté. Jedným z mechanizmov, ktorý môže viesť k dlhodobým zmenám na mozgu a spôsobovať zvýšenú náchylnosť na neuropsychiatrické ochorenia, je dysfunkcia hematoencefalickej bariéry. Zhao et al.31 injikovali poly(I:C) gravidným myšiam a preukázali narušenie hematoencefalickej bariéry plodu, ako aj jej narušenie v 6. mesiaci po narodení, čo v prípade myší zodpovedá dospelému veku.
Zvieracie modely však majú aj svoje značné limity. Jedným z nich je, že nezachycujú celú šírku prejavov PAS a schizofrénie, ako sa prezentujú u ľudí, ale len niektoré "im podobné črty". Je preto otázne, nakoľko sú poznatky zovšeobecniteľné na ľudskú populáciu. Navyše aj tieto výskumy prinášajú značne heterogénne výsledky na úrovni behaviorálnej i molekulovej, čo pravdepodobne súvisí s fázou gravidity a s veľkým počtom protektívnych a rizikových faktorov, ktoré vstupujú do hry a ktoré nie je možné naprieč štúdiami rovnako zohľadniť alebo ovplyvňovať, nakoľko zatiaľ ani nie sú známe.
PRENATÁLNY COVID-19 A RIZIKO VZNIKU PSYCHIATRICKÝCH OCHORENÍ - DISKUSIA K DOTERAJŠÍM POZNATKOM
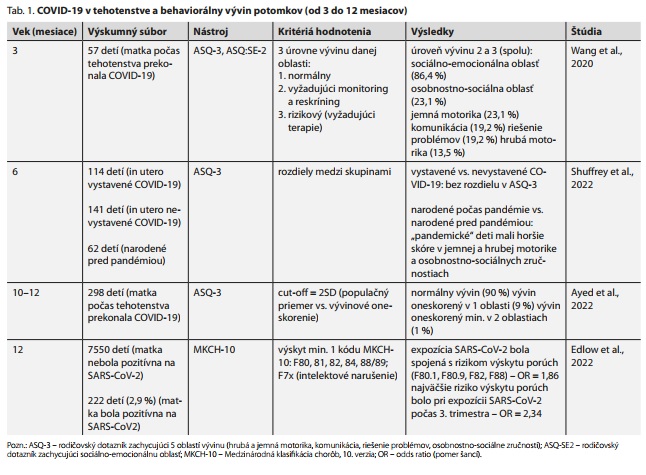
Na tomto mieste by sme mali zodpovedať otázku, ktorú sme položili v názve článku. Prinesie COVID-19 zvýšený výskyt PAS a schizofrénie, podobne ako v prípade epidémie rubeoly v USA? Vzhľadom na pomerne krátky čas od vypuknutia pandémie ochorenia COVID-19 zatiaľ neexistujú výskumy, ktoré by sledovali, ako jeho pôsobenie v tehotenstve súvisí s rizikom vzniku PAS alebo schizofrénie u potomkov. COVID-19 je vyvolaný vírusom SARS-CoV-2. Priebeh COVID-19 v populácii značne varíruje, niektorí infikovaní sú dokonca bez príznakov. Tehotné ženy sú náchylnejšie na infikovanie koronavírusom a rozvoj COVID-19.32 Nie je však známe, koľko žien na Slovensku alebo celosvetovo malo COVID-19 počas tehotenstva a koľko bolo bezpríznakových, napriek prítomnosti vírusu. Podľa štatistiky Centra pre kontrolu chorôb a prevenciu (CDC, 2022) do júla 2022 v USA prekonalo COVID-19 minimálne 225 000 tehotných žien, pričom takmer 35 000 podstúpilo hospitalizáciu.33 Údaje o hospitalizácii boli dostupné len u necelých 80 % žien z celkového počtu, takže počet hospitalizácií bol pravdepodobne ešte vyšší. Štúdia Edlowa et al.34 preukázala, že u tehotných žien s COVID-19 bola približne dvojnásobne vyššia pravdepodobnosť, že budú hospitalizované na jednotke intenzívnej starostlivosti a že budú ventilované, než u žien s COVID-19, ktoré neboli tehotné. Mortalita tehotných žien s COVID-19 však nebola významne vyššia.34 Ako sme uviedli vyššie, ak si prenatálna infekcia vyžaduje hospitalizáciu, riziko vzniku PAS u potomkov významne narastá.4 Doposiaľ bolo uskutočnených len niekoľko málo štúdií, ktoré sledovali, či COVID-19 počas tehotenstva ovplyvňuje správanie potomkov po narodení. Prehľad štyroch z nich prinášame v tab. 1.
Tri z týchto štúdií hodnotili správanie pomocou dotazníka ASQ-3 (Ages and Stages Questionnaires, Third Edition).35-37 Tento dotazník je postavený na výpovediach rodičov a mapuje päť oblastí vývinu: hrubá a jemná motorika, komunikácia, riešenie problémov, osobnostno-sociálne zručnosti. Wang et al.35 pomocou ASQ-3 sledovali v 3. mesiaci po narodení deti matiek, ktoré mali počas tehotenstva COVID-19. Pre každú oblasť stanovili tri stupne vývinu, v ktorom sa dieťa nachádza (1. normálny, 2. vyžadujúci ďalší monitoring a reskríning, 3. rizikový vyžadujúci terapie). Percento detí, u ktorých bol preukázaný 2. alebo 3. stupeň vývinu, sa pre jednotlivé oblasti pohybovalo od 13,5 % (hrubá motorika) po 23,1 % (jemná motorika a osobnostno-sociálna oblasť). Okrem ASQ-3 bola v tejto štúdii použitá aj škála pre sociálno-emocionálnu oblasť dotazníka ASQ-SE2 (Ages & Stages Questionnaires®: Social-Emotional, Second Edition). V tejto škále dosiahlo stupeň vývinu 2 a 3 až 86,4 % detí. Shuffrey et al.36 mapovali pomocou ASQ-3 v 6. mesiaci po narodení deti matiek, ktoré počas tehotenstva prekonali a neprekonali COVID-19. Medzi deťmi nezistili žiadne významné rozdiely. Hoci sa obe uvedené skupiny líšili v tom, či ich matka v tehotenstve prekonala COVID-19, spoločné mali to, že sa narodili počas pandémie. Keď porovnali stupeň vývinu oboch týchto skupín s deťmi, ktoré sa narodili ešte pred pandémiou, zistilo sa, že deti narodené počas pandémie mali významne nižšie skóre v oblasti jemnej a hrubej motoriky ako aj v osobnostno-sociálnych zručnostiach. Podľa tejto štúdie tak dôležitejší faktor vývinu bolo obdobie narodenia než prenatálne vystavenie ochoreniu. Ayed et al.37 sledovali pomocou ASQ-3 v 10-12. mesiaci po narodení deti matiek, ktoré v tehotenstve prekonali COVID-19. Ak v niektorej z oblastí dosiahlo dieťa skóre nižšie ako 2 smerodajné odchýlky, označili danú oblasť ako vývinovo oneskorenú. Ukázalo sa, že 90 % detí malo normálny vývin vo všetkých piatich oblastiach, 9 % detí malo vývinové oneskorenie v jednej oblasti, a len 1 % detí malo oneskorenie aspoň v dvoch oblastiach. Edlow et al.34 sledovali deti matiek, ktoré boli počas tehotenstva pozitívne testované na SARS-CoV-2, a matiek, ktoré boli testované negatívne. Zistili, že deti, ktorých matky boli v tehotenstve testované pozitívne, mali v 12. mesiaci po narodení významne vyššie riziko výskytu porúch motoriky alebo reči a jazyka podľa MKCH-10. Najvyššie riziko predstavovalo, ak bol vírus zistený počas 3. trimestra. Citované štúdie majú však svoj limity. Veľkosti sledovaných súborov sú väčšinou pomerne malé35,36 a niektoré štúdie nezahrnuli kontrolné súbory.35,37 Ďalej, ako sme uviedli, väčšina týchto štúdií použila dotazník ASQ-3, ktorý je postavený na výpovedi rodičov a nepredstavuje objektívne hodnotenie vývinovej úrovne dieťaťa. Objasnenie vzťahu medzi expozíciou ochorenia v tehotenstve a správaním po narodení si tak bude vyžadovať väčšie súbory, zohľadnenie ďalších faktorov, objektívne hodnotenie správania a dlhodobé sledovanie. Okrem kvalitných epidemiologických výskumov zatiaľ chýbajú aj animálne štúdie, ktoré by efekt koronavírusu počas tehotenstva na správanie potomkov overili experimentálne. SARS-CoV-2 predstavuje typ jednovláknového RNA vírusu. Vírusy, ako sme uviedli vyššie, sú v štúdiách nahrádzané injekciou poly(I:C), ktorá spúšťa cytokínovú kaskádu s preukázateľným efektom na neurovývin a behaviorálne parametre. V kaskáde figurujú najmä IL-6, TNF, IL-1β, IL-17, ktoré sa našli zvýšené aj u ľudí s COVID-19.38 Či však poly(I:C), ktorá imituje najmä účinky dvojvláknových RNA vírusov, je dobrým modelom v prípade jednovláknového SARS-CoV-2, je otázne. Navyše, okrem cytokínovej búrky sa možno v prípade SARS-CoV-2 uplatňujú aj iné mechanizmy. V kazuistickej štúdii bol dokonca zaznamenaný jeho prestup cez placentu u matky s COVID-19 v 35. týždni tehotenstva, pričom v tomto čase došlo k sekcii a následne rozvoju COVID-19 aj u dieťaťa.39 Viaceré štúdie však takýto priamy prestup vírusu nepotvrdili vôbec, alebo ho potvrdili len zriedkavo.38 Ďalej, ženy s COVID-19 počas tehotenstva majú zvýšené riziko infarktov placenty, čo môže viesť k nedostatočnému zásobovaniu plodu kyslíkom a živinami, a aj to môže prispieť k narušenému vývinu mozgu.32 V neposlednom rade je dôležité zvažovať aj vplyv psychosociálnej záťaže na priebeh tehotenstva, nakoľko tieto ženy uvádzali zvýšenú mieru anxiety, depresie a stresu spojenú so zmenami počas pandémie.32 Sumárne možno povedať, že z doposiaľ dostupných dát sa ukazuje, že tehotné ženy sú náchylnejšie na rozvinutie COVID-19, sú častejšie hospitalizované a ochorenie je sprevádzané cytokínovou búrkou. Uvedené faktory sú za určitých okolností rizikové pre rozvoj PAS a schizofrénie, ale definitívnu odpoveď na otázku, či to naozaj povedie k ich zvýšenému výskytu, prinesie až budúcnosť.
ZÁVER
Viaceré epidemiologické štúdie podporujú hypotézu, že infekcia matky počas tehotenstva zvyšuje riziko vzniku neuropsychiatrických porúch u exponovaných potomkov. Experimenty na zvieratách naznačujú, že kľúčovú úlohu zohráva aktivácia imunitného systému matky, a predovšetkým jeho produkty, cytokíny. Neurobiologický aj behaviorálny efekt infekcie však závisí od kombinácie mnohých rizikových a protektívnych faktorov, z ktorých viaceré ani nie sú známe, preto závery výskumov často nie sú jednotné. Sumárne, v prípade COVID-19 máme doposiaľ k dispozícii nasledovné poznatky. Tehotné ženy sú pravdepodobne náchylnejšie na vznik ochorenia COVID-19 a sú častejšie hospitalizované. Ochorenie je sprevádzané cytokínovou búrkou, môže spôsobovať infarkty placenty a nedostatočné zásobovanie plodu kyslíkom a živinami. Zriedkavo môže dochádzať aj k priamemu prestupu vírusu cez placentu. Navyše, matky zažívajú vyššiu mieru negatívnych emócií, čo môže viesť k oslabeniu ich imunitného systému a podpore zápalu. Ako ukázali výskumy na iných typoch infekcií, uvedené faktory sa spájajú so zvýšeným rizikom PAS a schizofrénie. Môžeme preto vysloviť hypotézu, že COVID-19 prekonaný počas tehotenstva bude spojený s určitým rizikom vzniku PAS, schizofrénie, prípadne iného psychiatrického ochorenia u exponovaného plodu. V prípade COVID-19 však pochopiteľne zatiaľ chýbajú epidemiologické štúdie, ktoré by túto imunologickú hypotézu etiológie neuropsychiatrických porúch overili. Doterajšie behaviorálne štúdie, ktoré skúmali správanie detí prenatálne vystavených COVID-19, zatiaľ priniesli nekonzistentné výsledky, mali rôzne metodologické nedostatky, a navyše boli uskutočnené len do prvého roku života detí. Rovnako chýba adekvátna náhrada jednovláknových RNA vírusov, ktorá by v animálnych modeloch napodobnila efekt SARS-CoV-2. Odpoveď na nami položenú otázku je tak nateraz v rovine hypotézy a jasnú odpoveď nám dá až budúcnosť. Najbližšie roky tak v tejto oblasti predstavujú výzvu pre výskum i klinickú prax.
LITERATÚRA
- 1. Murray RM, Bhavsar V, Tripoli G, Howes O. 30 Years on: How the Neurodevelopmental Hypothesis of Schizophrenia Morphed Into the Developmental Risk Factor Model of Psychosis. Schizophrenia Bulletin 2017; 43 (6): 1190-1196.
- 2. Shook LL, Sullivan EL, Jamie OL, Perlis RH, Edlow AG. COVID-19 in pregnancy: implications for fetal brain development. Trends Mol Med 2022; 28 (4): 319-330.
- 3. Hutton J. Does Rubella Cause Autism: A 2015 Reappraisal? Frontiers in Human Neuroscience 2016; 10: 25.
- 4. Jiang HY, Xu LL, Shao L et al. Maternal infection during pregnancy and risk of autism spectrum disorders: A systematic review and meta-analysis. Brain Behavior and Immunity 2016; 58: 165-172.
- 5. Hornig M, Bresnahan MA, Che X et al. Prenatal fever and autism risk. Molecular Psychiatry 2018; 23 (3): 759-766.
- 6. Brucato M, Ladd-Acosta C, Li M et al. Prenatal exposure to fever is associated with autism spectrum disorder in the boston birth cohort. Autism Research 2017; 10 (11): 1878-1890.
- 7. Tioleco N, Silberman AE, Stratigos K et al. Prenatal maternal infection and risk for autism in offspring: A meta-analysis. Autism Research 2021; 14 (6): 12961316.
- 8. Brynge M, Sjoqvistt H, Gardner RM et al. Maternal infection during pregnancy and likelihood of autism and intellectual disability in children in Sweden: a negative control and sibling comparison cohort study. The Lancet Psychiatry 2022. 9 (10): 782-791.
- 9. Zhou YY, Zhang WW, Chen F, Hu SS, Jiang HY. Maternal Infection Exposure and the Risk of Psychosis in the Offspring: A Systematic Review and Meta-Analysis. Journal of Psychiatric Research 2021; 135: 28-36.
- 10. Brown AS, Derkits EJ. Prenatal Infection and Schizophrenia: A Review of Epidemiologic and Translational Studies. The American Journal of Psychiatry 2010; 167 (3): 261-280.
- 11. Ellman LM, Yolken RH, Buka SL, Torrey EF, Cannon TD. Cognitive Functioning Prior to the Onset of Psychosis: The Role of Fetal Exposure to Serologically Determined Influenza Infection. Biological Psychiatry 2009; 65 (12): 1040-1047.
- 12. Cheslack-Postava K, Brown AS. Prenatal Infection and Schizophrenia: A Decade of Further Progress. Schizophrenia Research 2022; 247: 7-15.
- 13. Blomstrom A, Karlsson H, Wicks S et al. Maternal Antibodies to Infectious Agents and Risk for Non-Affective Psychoses in the Offspring - a Matched Case-Control Study. Schizophrenia Research 2012; 140 (1): 25-30.
- 14. Brown AS. Exposure to Prenatal Infection and Risk of Schizophrenia. Frontiers in Psychiatry 2011; 2: 63.
- 15. Brown AS, Cohen P, Harkavy-Friedman J et al. A.E. Bennett Research Award. Prenatal Rubella, Premorbid Abnormalities, and Adult Schizophrenia. Biological Psychiatry 2001; 49 (6): 473-486.
- 16. Lee YH, Cherkerzian S, Seidman LJ et al. Maternal Bacterial Infection During Pregnancy and Offspring Risk of Psychotic Disorders: Variation by Severity of Infection and Offspring Sex. American Journal of Psychiatry 2020; 177 (1): 66-75.
- 17. Nielsen PR, Laursen TM, Mortensen PB. Association between Parental Hospital-Treated Infection and the Risk of Schizophrenia in Adolescence and Early Adulthood. Schizophrenia Bulletin 2013; 39 (1): 230-237.
- 18. Brown AS, Schaefer CA, Quesenberry CP et al. Maternal Exposure to Toxoplasmosis and Risk of Schizophrenia in Adult Offspring. The American Journal of Psychiatry 2005; 162 (4): 767-773.
- 19. Mortensen PB, N0rgaard-Pedersen B, Waltoft BL et al. Toxoplasma Gondii as a Risk Factor for Early-Onset Schizophrenia: Analysis of Filter Paper Blood Samples Obtained at Birth. Biological Psychiatry 2007; 61 (5): 688-693.
- 20. Xiao J, Buka SL, Cannon TD et al. Serological Pattern Consistent with Infection with Type I Toxoplasma Gondii in Mothers and Risk of Psychosis among Adult Offspring. Microbes and Infection 2009; 11 (13): 1011-1018.
- 21. Norouzi M, Tabaei SJS, Niyyati M, Saber V, Behniafar H. Genotyping of Toxoplasma Gondii Strains Isolated from Patients with Ocular Toxoplasmosis in Iran. Iranian Journal of Parasitology 2016; 11 (3): 316-324.
- 22. Ashdown H, Dumont Y, Ng M et al. The role of cytokines in mediating effects of prenatal infection on the fetus: implications for schizophrenia. Molecular Psychiatry 2006; 11 (1): 47-55.
- 23. Oskvig DB, Elkahloun AG, Johnson KR, Phillips TM, Herkenham M. Maternal immune activation by LPS selectively alters specific gene expression profiles of interneuron migration and oxidative stress in the fetus without triggering a fetal immune response. Brain, Behavior and Immunity 2012; 26 (4): 623-634.
- 24. Arrode-Bruses G, Bruses JL. Maternal immune activation by poly I: C induces expression of cytokines IL-10 and IL-13, chemokine MCP-1 and colony stimulating factor VEGF in fetal mouse brain. Journal of Neuroinflammation 2012; 9: 83.
- 25. Woods RM, Lorusso JM, Potter HG et al. Maternal immune activation in rodent models: A systematic review of neurodevelopmental changes in gene expression and epigenetic modulation in the offspring brain. Neuroscience and Biobehavioral Reviews 2021; 129: 389-421.
- 26. Allswede DM, Yolken RH, Buka SL, Cannon TD. Cytokine concentrations throughout pregnancy and risk for psychosis in adult offspring: a longitudinal case-control study. Lancet Psychiatry 2020; 7 (3): 254-261.
- 27. Meyer U, Feldon J, Yee BK. A review of the fetal brain cytokine imbalance hypothesis of schizophrenia. Schizophrenia Bulletin 2009; 35 (5): 959-972.
- 28. Mousa A, Bakhiet M. Role of Cytokine Signaling during Nervous System Development. International Journal of Molecular Sciences 2013; 14 (7): 1393113957.
- 29. Bilbo SD, Schwarz JM. The immune system and developmental programming of brain and behavior. Frontiers in Neuroendocrinology 2012; 33 (3): 267-286.
- 30. Meyer U. Neurodevelopmental Resilience and Susceptibility to Maternal Immune Activation. Trends in Neurosciences 2019; 42 (11): 793-806.
- 31. Zhao Q, Dai W, Chen HY. Prenatal disruption of blood-brain barrier formation via cyclooxygenase activation leads to lifelong brain inflammation. Proc Natl Acad Sci USA 2022; 119 (15): e2113310119.
- 32. Holland C, Hammond C, Richmond MM. COVID-19 and Pregnancy: Risks and Outcomes. Nursing for Women´s Health 2023; 27 (1): 31-41.
- 33. Centers for Disease Control and Prevention Data on COVID-19 during pregnancy: Severity of maternal illness. 2022. https://stacks.cdc.gov/view/cdc/119588
- 34. Edlow AG, Castro VM, Shook LL, Kaimal AJ, Perlis R. Neurodevelopmental Outcomes at 1 Year in Infants of Mothers Who Tested Positive for SARS-CoV-2 During Pregnancy. JAMA network open 2022; 5 (6): e2215787.
- 35. Wang Y, Chen L, Wu T et al. Impact of Covid-19 in pregnancy on mother´s psychological status and infant´s neurobehavioral development: a longitudinal cohort study in China. BMC Medicine 2020; 18 (1).
- 36. Shuffrey LC, Firestein MR, Kyle MH et al. Association of Birth During the COVID-19 Pandemic With Neurodevelopmental Status at 6 Months in Infants With and Without In Utero Exposure to Maternal SARS-CoV-2 Infection. JAMA Pediatrics 2022; 176 (6): e215563.
- 37. Ayed M, Embaireeg A, Kartam M et al. Neurodevelopmental outcomes of infants born to mothers with SARS-CoV-2 infections during pregnancy: a national prospective study in Kuwait. BMC Pediatrics 2022; 22 (1): 319.
- 38. Granja MG, Oliveira ACR, Figueiredo CS et al. SARS-CoV-2 Infection in Pregnant Women: Neuroimmune-Endocrine Changes at the Maternal-Fetal Interface. Neuroimmunomodulation 2021; 28 (1): 1-21.
- 39. Vivanti AJ, Vauloup-Fellous C, Prevot S et al. Transplacental transmission of SARS-CoV-2 infection. Nature Communications 2020; 11: 3572.
- 40. Estes ML, McAllister AK. Maternal immune activation: Implications for neuropsychiatric disorders. Science 2016; 353 (6301): 772-777.





