Česká a slovenská psychiatrie

Časopis
Psychiatrické společnosti ČLS JEP
a Psychiatrickej spoločnosti SLS
souborný článek / review article
PSYCHIATRICKÉ KOMPLIKACE PŘI LÉČBĚ KORTIKOIDY
PSYCHIATRIE ADVERSE EFFECTS OF CORTICOSTEROID TREATMENT
David Kolouch1, Michal Goetz1
1 Dětská psychiatrická klinika 2. LF UK a FN v Motole, Praha
SOUHRN
Kolouch D, Goetz M. Psychiatrické komplikace při léčbě kortikoidy
Psychiatrické komplikace představují časté nežádoucí účinky kortikoidní léčby u dětských i dospělých pacientů. Kortizol hraje důležitou roli v metabolismu buněk a udržování homeostázy organismu. Podávání exogenních kortikoidů vede k potlačení tvorby endogenního kortizolu a nerovnováze mezi aktivitou glukokortikoidních a mineralokortikoidních receptorů, což je zřejmě podkladem narušení kognitivních funkcí a emoční dysregulace. Nežádoucí účinky se projevují širokým spektrem psychiatrických symptomů a syndromů různého stupně závažnosti od afektivních a úzkostných poruch, psychotických poruch a delirantních stavů, až po narušení kognitivních funkcí. Rovněž je významně zvýšeno riziko suicidálního jednání. Mohou se manifestovat kdykoliv během léčby nebo krátce po jejím skončení, přičemž nejčastěji dochází k jejich rozvoji během počátečních dvou týdnů léčby. Ohrožené vznikem komplikací jsou zejména mladší děti a starší pacienti. Hlavním rizikovým faktorem je vysoká dávka kortikoidů, avšak riziko vzniku komplikací nelze vyloučit ani při podávání velmi nízkých dávek kortikoidů. Zvýšené riziko představují onemocnění spojená s hypoalbuminémií (např. nefrotický syndrom) a s narušením hematoencefalické bariéry (např. SLE). Dalšími rizikovými faktory jsou přítomnost primárního psychiatrického onemocnění v anamnéze a předchozí psychiatrické komplikace po podání kortikoidů, nezanedbatelná je i možnost interakcí s ostatními léky na cytochromu P450. Je pravděpodobné, že dlouhodobě působící kortikoidy (např. dexamethason) způsobují častější psychiatrické komplikace oproti kortikoidům s kratším biologickým poločasem (např. prednison). Strategie léčby jsou založeny převážně na jednotlivých kazuistických sděleních či sériích kazuistik První krokem má být snížení dávky či vysazení kortikoidního preparátu z medikace pacienta, pakliže to primární onemocnění pacienta umožňuje. Pokud redukce dávky kortikoidů není možná nebo není dostačující ke zvládnutí obtíží, je indikováno zahájení specifické psycho-farmakologické léčby. U depresivity je vhodné nasazení antidepresiv typu SSRI, v případě psychotické deprese je prokázán efekt antipsychotik a elektrokonvulzivní terapie. Při podezření na bipolaritu je vhodné nasazení stabilizátorů nálady či atypických antipsychotik. Profylaktické podávání psychofarmak je doporučeno pouze při nutnosti podávat kortikoidy pacientům s anamnézou již proběhlé steroidní psychózy či epizody mánie. Klíčovou složkou prevence je dostatečná informovanost lékařů a důsledná edukace pacientů o riziku rozvoje nežádoucích účinků.
Klíčová slova: kortikoidy, dexamethason, prednison, nežádoucí účinky, děti, dospělí, rizikové faktory, léčba
SUMMARY
Kolouch D, Goetz M. Psychiatrie adverse effects of corticosteroid treatment
Psychiatrie complications are frequent side effects of corticosteroid therapy in pediatrie and adult patients. Cortisol plays an important role in the cell metabolism and in maintaining the homeostasis. Administration of exogenous corticosteroids leads to the suppression of endogenous cortisol secretion and causes an imbalance between glucocorticoid and mineralocorticoid receptor activity. It is hypothesized that this is the underlying mechanism of the disruption of cognitive functions and emotional dysregulation. Adverse events are manifested by a wide range of psychiatric symptoms and syndromes, of varying degrees of severity. These include disruption of cognitive functions, affective and anxiety disorders, psychotic disorders and delirious states. They also significantly increase the risk of suicidal behavior. They may onset at any time during corticosteroids use with the most frequent occurrence during the first two weeks of treatment. Younger children and the elderly patients are at highest risk. The main risk factor is a high dose of corticosteroids, however complications cannot be ruled out even when administering very low doses. Somatic risk factors include hypoalbu-minemia (eg. nephrotic syndrome) and the disruption of the blood-brain barrier (eg. Systemic Lupus Erythematosus). Other predisposing factors include a history of primary psychiatric disorder, previous psychiatric complications after corticosteroid use, and concomitant medication causing the interactions on the cytochrome P450. Long-acting corticosteroids (eg. dexamethasone) are likely to cause more frequent psychiatrie complications than those with shorter half-life (eg. prednisone). Treatment strategies are based largely on individual case reports or case series. The first step is to reduce the dose or withdraw the corticosteroid if the primary illness allows. If corticosteroid dose reduction is not possible or not sufficient to cope with psychiatric symptoms, the initiation of specific psychopharmacological treatment is indicated. For depression, it is advisable to use SSRI antidepressants, in the case of psychotic depression, the effect of both atypical antipsychotics and electrocon-vulsive therapy has been demonstrated. When bipolar disorder is suspected, the use of mood stabilizers or atypical antipsychotics is recommended. Prophylactic use of medication is reserved for patients with a history of steroid psychosis or episodes of mania. A key component of prevention is the adequate awareness of professionals and consistent education of patients about the risk of developing side effects.
Key words: corticosteroids, dexamethasone, prednisone, side effects, children, adults, risk factors, treatment
ÚVOD
Kortikoidy jsou velmi často užívanou lékovou skupinou jak během dětství, tak i v dospělém věku. Kromě specifického užití v neonatální medicíně jsou kortikoidy nezastupitelnou součástí léčebných protokolů řady autoimunitních, dermatologických, endokrinních, hemato onkologických, neurologických, revmatologických a očních onemocnění. Kortikoidy jsou užívány jak krátkodobě ke zvládnutí akutních stavů, tak i při dlouhodobé léčbě chronických onemocnění trvajících řadu měsíců i let. Přes jejich nezpochybnitelnou účinnost a nezastupitelnost v terapii těchto onemocnění je jejich užití spojeno s mnoha nežádoucími účinky. Zatímco somatickým nežádoucím účinkům je v literatuře věnována relativně velká pozornost, o možných psychiatrických nežádoucích účincích kortikoidů je toho publikováno nesrovnatelně méně. Cílem tohoto článku je představit aktualizovaný soubor informací na téma psychiatrických nežádoucích účinků u dětských i dospělých pacientů, shrnout postupy léčby těchto stavů a nastínit možné způsoby jejich prevence.
MECHANISMUS VZNIKU NEŽÁDOUCÍCH ÚČINKŮ
Kortizol jako hlavní endogenní glukokortikoid hraje důležitou roli v metabolismu buněk, je nezbytný k udržení homeostázy našeho organismu během stresové reakce a má důležitý vliv na emoce, paměť a kognici. Působením stresu dochází v hypotalamu k sekreci kortikoliberinu, který stimuluje uvolňování adrenokortikotropinu v předním laloku hypofýzy, což vede k uvolnění kortizolu a kortikosteronu z nadledvin. Kromě vlivu na genovou expresi buněk má kortizol rovněž i rychlé negenomické účinky, které jsou zprostředkované vazbou kortizolu na glukokortikoidní a mineralokortikoidní receptory buněk. Mineralokortikoidní receptory jsou nutné k vyhodnocení podnětu a nástupu stresové reakce, glukokortikoidní receptory jsou aktivovány až vyšší hladinou steroidních hormonů a jsou odpovědné za její ukončení. Podání exogenního kortikoidu vede k potlačení tvorby endogenního kortizolu a následné nerovnováze mezi aktivitou glukokortikoidních a mineralokortikoidních receptorů, což je pravděpodobným podkladem narušení kognitivních funkcí a emoční regulace během kortikoidní terapie.1 Dlouhodobá expozice vysokým dávkám kortikosteroidů u zvířecích modelů potlačuje větvení dendritů ("branching") a axonální pučení ("sprouting") v určitých oblastech mozku, což vede k narušení procesů regenerace neuronálního poškození.2,3 Kromě toho glukokortikoidy snižují dostupnost glukózy v hipokampu,4 u zvířecích modelů rovněž potlačují tvorbu neurotrofických faktorů v hipokampu a neokortexu.5,6 Snížená exprese neurotrofických faktorů v těchto oblastech se podle Dumaná může podílet na rozvoji deprese.7 Narušení kognitivních funkcí při léčbě kortikoidy je zřejmě důsledkem dlouhodobého působení kortikoidu na mineralokortikoidní a glukokortikoidní receptory v oblasti hipokampu a zmenšení jeho objemu,8 de Quervain dále popisuje zhoršení deklarativní paměti při poklesu krevního průtoku v mediální části temporálního laloku následkem akutního podání kortikoidu zdravým dobrovolníkům.9 Dlouhodobé podávání glukokortikoidů je pak spojeno s menším hipokampálním objemem a nižší hladinou N-acetylaspartátu (markeru neuronální viability) u pacientů v kortikoidní skupině.
INCIDENCE A PREZENTACE NEŽÁDOUCÍCH ÚČINKŮ
Psychiatrické nežádoucí účinky kortikoidní léčby představují celé spektrum symptomů a syndromů různého stupně závažnosti. Většina publikovaných dat se pohybuje na úrovni kazuistik, proto je přesnější stanovení incidence psychiatrických nežádoucích účinků v pediatrické populaci poměrně komplikované. V jedné rozsáhlejší studii sledující incidenci mezi 1603 pacienty léčenými kortikoidy pro akutní lymfoblastickou leukémii popisuje Mitchell behaviorální nežádoucí účinky u 6 % pacientů medikovaných dexamethazonem, přičemž mezi nejčastější komplikace patřily zejména prudké výkyvy nálad, emoční labilita, deprese a nárůst agresivního chování, pozorováno bylo rovněž několik případů rozvoje psychózy. Z hlediska pohlaví dívky vykazovaly sklon k depresivnímu prožívání, u chlapců byl patrný spíše nárůst agresivního chování.10 Rovněž údaje od dalších autorů svědčí pro nárůst úzkostně-depresivního prožívání,11,12 agresivního chování a narušení pozornosti.12,13 Opakovaně byla u dětí na kortikoidní medikaci zaznamenána zvýšená plačtivost, podrážděnost a tendence k odmlouvání, narušení emoční regulace a nespavost, přičemž tyto akutní účinky na chování a náladu mohou být výraznější u mladších dětí v předškolním věku.14 Jednotlivá kazuistická sdělení pak popisují rozvoj psychotické mánie,15 obsedantně-kompulzivní poruchy,16 opakovaně je popisována nespavost, emoční labilita a výbuchy vzteku. Výsledky studií sledujících vliv kortikoidu na kognitivní funkce u dětí ukazují na možné narušení deklarativní paměti,14 nicméně dosavadní výsledky jsou nejednoznačné a je třeba dalšího výzkumu v této oblasti.
Rovněž u dospělých pacientů je popisováno celé spektrum psychiatrických komplikací jako důsledek akutního či chronického užívání kortikoidu. V udávané incidenci však mezi jednotlivými autory existují poměrně velké rozdíly. Ty jsou podle Warringtona důsledkem nepředvídatelného rozvoje nežádoucích účinků, rozdílných kritérií pro jejich definici a klasifikaci, širokého spektra užívaných typů kortikoidu a jejich dávek, roli hrají rovněž i rozdíly mezi skupinami sledovaných pacientů.17 Lewis a Smith v metaanalýze 935 dospělých pacientů z 11 nekontrolovaných studií udávají celkovou incidenci mezi 13 a 62 % (vážený průměr 27,6 %) komplikací převážně lehkého až středního stupně závažnosti.18 V další metaanalýze nekontrolovaných studií zahrnující 2555 dospělých pacientů léčených kortikoidy pro různé diagnózy uvádějí stejní autoři průměrnou incidenci 5,7 % závažných psychiatrických komplikací.18 Naber et al. v nekontrolované prospektivní studii u 50 pacientů léčených krátkodobě vysokou dávkou kortikoidu pro oční onemocnění zaznamenali u 36 % pacientů rozvoj manických nebo depresivních obtíží různého stupně závažnosti.19 Dlouhodobé podávání malých dávek kortikoidu je podle Sandry Bolanos spojeno s kumulativním 60% rizikem rozvoje poruchy nálady či úzkostné poruchy.20 Tato data jsou konzistentní s nálezy u pacientů s Cushingovou chorobou, kde při excesivní nadprodukci endogenního kortizolu patří poruchy nálady a úzkostné poruchy k nejčastějším psychiatrickým komorbiditám.21 Laurence Fardetová srovnávala výskyt pěti závažných neuropsychiatrických komplikací u 261 272 pacientů užívajících po dobu 3 měsíců kortikoidy s kontrolní skupinou pacientů se stejným somatickým onemocněním, avšak bez kortikoidu v medikaci. Pacienti léčení kortikoidy měli dvojnásobně zvýšené riziko rozvoje deprese, čtyř- až pětinásobně zvýšené riziko rozvoje mánie či delirantního stavu. Riziko suicidálního pokusu či dokonaného suicidia pak vzrostlo téměř sedminásobně.22 Výzkumy sledující ovlivnění kognitivních funkcí pak ukazují na přechodné zhoršení deklarativní paměti vlivem kortikoidní medikace.23
DOBA NÁSTUPU NEŽÁDOUCÍCH ÚČINKŮ
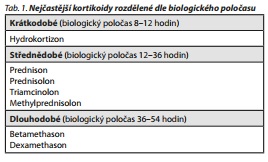
V pediatrické literatuře chybějí významnější studie sledující časovou osu rozvoje nežádoucích účinků. Podle řady kazuistických sdělení a výsledků francouzské farmakovigilanční skupiny24 dochází u dětí k rozvoji nežádoucích účinků nejčastěji během prvního týdne užívání, obvykle bezprostředně po zahájení medikace nebo během několika dnů od začátku jejího užívání.15 Rovněž u dospělých pacientů je popisován rychlý nástup nežádoucích účinků. Lewis a Smith udávají medián do nástupu nežádoucích účinků 11,5 dne, přičemž 39 % komplikací se rozvinulo během prvního týdne, 62 % během prvních 14 dnů a 83 % během počátečních 6 týdnů od zahájení kortikoidní medikace.18 Sirois popisuje bimodální rozložení manifestace komplikací v čase s výskytem časných komplikací kolem čtvrtého dne od zahájení užívání a tzv. pozdních komplikací kolem třetího týdne trvání léčby. 25 Ve shodě s předešlými autory uvádějí Naber et al. u 50 oftalmologických pacientů rozvoj komplikací během prvních 3 dnů od zahájení léčby.19 Nishimura udává průměrnou dobu do manifestace nežádoucích účinků kolem 12 dnů,26 rovněž i Ling popisuje rozvoj komplikací během několika dnů až prvních dvou týdnů léčby.27 Vzhledem k dlouhým poločasům dexamethasonu a betamethasonu kolem 36-54 hodin (tab. 1) byl zaznamenán i rozvoj nežádoucích účinků až s časovým odstupem po užití poslední dávky kortikoidu.28
ROZDÍLY MEZI GLUKOKORTIKOIDY
Je pravděpodobné, že dexamethason ve srovnání s prednisonem způsobuje častěji nežádoucí účinky. Mitchell ve své studii zahrnující přes 1600 pacientů udává 6% výskyt behaviorálních nežádoucích účinků u subjektů léčených dexamethasonem, ve srovnání s 1% výskytem komplikací u pacientů užívajících prednison. Pacienti, u kterých došlo k rozvoji závažnějších behaviorálních nežádoucích účinků při užívání dexamethasonu, a byli proto převedeni na prednison, nejevili po změně medikace žádné významnější behaviorální nežádoucí účinky.10 Tyto závěry je však třeba posuzovat s opatrností, neboť studie nebyla zaslepená a ošetřující lékaři byli informováni o zařazení pacientů do jednotlivých skupin. Podle výsledků metaanalýzy 8 randomizovaných studií srovnávajících dexamethason s prednisonem v indukční fázi léčby ALL u dětí je riziko neuropsychiatrických komplikací u dexamethasonu zvýšené více než čtyřnásobně ve srovnání s prednisonem, Teuffel jako možné vysvětlení uvádí lepší prostupnost tkáně CNS pro dexamethason.29 Podle závěrů jiné kontrolované studie je u pacientů na dexamethasonu pozorováno častější přejídání a pocity hladu s následnou podrážděností oproti pacientům užívajícím prednison.30 Konečně podle Fardetové dlouhodobě působící glukokortikoidy (dexamethason, betamethason) významně zvyšují riziko rozvoje deprese navozené vysazením kortikoidu ve srovnání s kortikoidy s kratším biologickým poločasem (prednison, prednisolon, methylprednisolon).22 Inhalační cesta podání kortikoidu je ve srovnání se systémovým podáním spojena s menší pravděpodobností rozvoje nežádoucích účinků, avšak ani zde riziko nelze zcela vyloučit. Silverman ve studii u 1981 dětí ve věku 5-10 let s lehkým astmatem srovnával riziko nežádoucích účinků mezi skupinou dětí užívající budesonid a placebovou skupinou, přičemž zaznamenal nežádoucí psychiatrické reakce u méně než 0,5 % dětí v obou skupinách a jednalo se převážně o méně závažné komplikace.31 Kazuisticky byl však popsán i rozvoj psychotické mánie u šestnáctileté dívky po zahájení inhalačního podávání beclomethasonu.15
DÁVKA A RIZIKO NEŽÁDOUCÍCH ÚČINKŮ
Dávka kortikoidu je nejdůležitějším rizikovým faktorem. V pediatrické literatuře bohužel neexistují dostatečně významná data sledující závislost dávky kortikoidu a rizika rozvoje nežádoucích účinků. U dospělých došlo dle výsledků multicentrické prospektivní studie Bostonské skupiny pro spolupráci při sledování nežádoucích účinků léčiv k rozvoji akutních psychiatrických nežádoucích účinků u 1,3 % pacientů užívajících do 40 mg prednisonu za den, u 4,6 % pacientů užívajících 41-80 mg prednisonu za den a u 18,4 % pacientů užívajících více než 80 mg prednisonu denně,17 vztah dávky kortikoidu k riziku rozvoje nežádoucích účinků potvrzují i novější studie. 22 Zajímavé je, že nebyl prokázán vztah mezi dávkou kortikoidu a délkou trvání ani závažností komplikací. V literatuře nalezneme i případy rozvoje psychotického stavu po podání velmi nízkých dávek kortikoidu.32,33
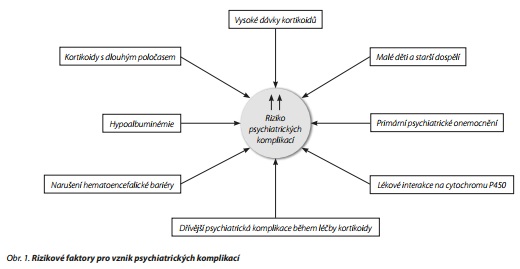
DALŠÍ RIZIKOVÉ FAKTORY
Kromě dávky kortikoidu existují i další významné rizikové faktory (obr. 1). Ve starší literatuře je u dospělých pacientů popisováno zvýšené riziko rozvoje psychiatrických komplikací u žen,18 nicméně další studie naopak svědčí proti rozdílům v incidenci mezi oběma pohlavími.19 Je však zřejmé, že jednotlivé psychiatrické komplikace se vyskytují u obou pohlaví s různou četností. Fardetová u dospělých žen pozorovala zvýšené riziko deprese, u mužů pak vyšší riziko rozvoje mánie a delirantního stavu. Riziko deprese, mánie a deliria se u dospělých pacientů podle Fardetové zvyšovalo s věkem, zatímco riziko panické ataky a suicidalita byly vyšší u mladších pacientů. U dívek léčených kortikoidy pro akutní lymfoblastickou leukémii Mitchell pozoroval vyšší riziko depresivity, u chlapců pak zvýšené riziko agresivního chování.10 Větší vnímavost k neuropsychiatrickým komplikacím je v pediatrické literatuře popisována u mladších dětí kolem předškolního věku.14 Na rozdíl od výsledků starších studií34 je podle Fardetové pozitivní anamnéza psychiatrického onemocnění spojena se zvýšeným rizikem vzniku psychiatrických komplikací během terapie kortikoidy.22 Fardetová toto vysvětluje jako možnou predispozici jedince k rozvoji daného psychiatrického onemocnění, které se může opětovně manifestovat během kortikoidní léčby. Pozoruhodné je, že dříve absolvovaná kortikoidní terapie je u pacientů spojovaná s nižším rizikem rozvoje nových psychiatrických komplikací. Za nejpravděpodobnější považuje Fardetová vysvětlení, že pacientům s anamnézou proběhlé nežádoucí reakce byly kortikoidy znovu předepisovány s podstatně menší frekvencí. Riziko výskytu nežádoucích účinků kortikoidu je rovněž vyšší u některých somatických onemocnění. V pediatrické literatuře nalezneme častější rozvoj psychiatrických komplikací u pacientů s nefrotickým syndromem, u dospělých je pak zvýšené riziko zaznamenáno i u pacientů s chronickou aktivní hepatitidou doprovázenou hypoalbuminémií. Podle výsledků farmakokinetických studií dochází během epizody hypoalbuminémie ke zvýšení volné frakce prednisolonu v séru, což je poté příčinou zvýšené frekvence nežádoucích účinků.35 Dalším faktorem zvyšujícím riziko rozvoje nežádoucích účinků je narušení hematoencefalické bariéry, ke kterému dochází u pacientů se systémovým lupus erythematodes.26 Jiné kazuistiky popisují případy rozvoje psychózy, resp. mánie při současném užívání prednisonu s klarithromycinem, významným inhibitorem enzymu CYP3A. Interakce léků na úrovni cytochromu P450 s následnou inhibicí metabolismu kortikoidu vede podle autorů ke zvýšení hladiny volného prednisolonu v plazmě a zvýšení rizika manifestace nežádoucích účinků.36,37
LÉČBA A ZVLÁDÁNÍ KOMPLIKACÍ
Strategie zvládání psychiatrických nežádoucích účinků jsou založeny převážně na jednotlivých kazuistických sděleních či sériích kazuistik První krokem v případě závažných nežádoucích účinků by vždy mělo být zvážení redukce dávky až úplného vysazení glukokortikoidu, pakliže to vývoj primárního onemocnění pacienta umožňuje. Většina nežádoucích účinků postupně odeznívá spontánně po vysazení nebo snížení dávky kortikoidu.17 Zejména v případech dlouhodobého užívání glukokortikoidu je důležité respektovat schéma postupného vysazování, během něhož by měl být pacient sledován pro riziko rozvoje či prohloubení depresivity nebo delirantního stavu.38 V případech, kdy dojde během detitrace glukokortikoidu k rozvoji deprese a únavy, je nutné vyloučit možný útlum hormonální sekrece na ose hypotalamus-hypofýza-nadledviny a ev. včas zahájit substituční léčbu. Pokud redukce dávky kortikoidu není s ohledem na primární onemocnění pacienta možná nebo není vzhledem k závažnosti psychiatrických komplikací dostačující, je vhodné zahájení specifické psychofarmakologické léčby. Při úzkostné a depresivní symptomatice je vhodné nasazení selektivních inhibitorů zpětného vychytávání serotoninu (sertralin, fluoxetin, citalopram) nebo venlafaxinu, tricyklická antidepresiva jsou podle některých autorů spojena s nárůstem agitovanosti a prohloubení psychotické alterace.39 U psychotické deprese indukované glukokortikoidy byl kromě antipsychotik rovněž prokázán příznivý efekt elektrokonvulzivní terapie.40 Při podezření na bipolaritu je namísto antidepresiva vhodné nasazení stabilizátorů nálady k prevenci přesmyku do manických nebo smíšených fází. Rada kazuistik u dospělých pacientů popisuje příznivý efekt lithia a karbamazepinu.17 Vzhledem k riziku hematologických nežádoucích účinků a interakcí těchto thymoprofylaktik s chemoterapií je však zejména u dětských onkologických pacientů v případech mánie či psychózy vhodnější užití atypických antipsychotik.41 V dostupné literatuře najdeme zprávy o účinnosti risperidonu, olanzapinu, aripiprazolu a quetiapinu.41-43 V případě výrazného neklidu pak lze rovněž kombinovat s benzodiazepiny. U delirií je popisováno úspěšné užití haloperidolu nebo atypických antipsychotik.40
MOŽNOSTI PREVENCE KOMPLIKACÍ
Profylaktická léčba nežádoucích účinků by měla být zvažována pouze ve specifických případech při nutnosti podávat kortikoidy pacientům s anamnézou proběhlé steroidní psychózy či epizody mánie. Na základě omezeného množství důkazů lze usuzovat, že profylaxe v indikovaných případech pomáhá snižovat riziko vzniku budoucích psychiatrických komplikací. Jedním z nejdéle užívaných profylaktik kortikoidních nežádoucích účinků je lithium. Podle výsledků otevřené studie u dospělých pacientů s roztroušenou sklerózou léčených kortikotropinem profylaktické podávání lithia významně snížilo riziko rozvoje psychózy.44 Účinnost lithia popisuje i řada kazuistických sdělení,45 významnější randomizované studie podporující tuto hypotézu však chybějí. Kazuistická sdělení vypovídají rovněž o profylaktickém efektu na poruchy nálady a psychotickou alteraci u chlorpromazinu, valproátu a lamotriginu. V rámci prevence přechodného zhoršení deklarativní paměti doprovázející terapii kortikoidy byl s úspěchem podáván lamotrigin a memantin.46,47
Klíčovou složkou prevence je především dostatečná informovanost lékařů a edukace pacientů o možném riziku rozvoje psychiatrických nežádoucích účinků v souvislosti s užíváním kortikoidů. Podle McGrathové představovaly psychiatrické komplikace související s kortikoidní medikací největší zdroj stresové zátěže pro rodiny dětí podstupujících udržovací fázi léčby akutní lymfoblastické leukémie.48 Z tohoto pohledu se může zdát poněkud překvapivé, že mnoho pacientů se i přesto zdráhá svěřit svému lékaři s obtěžujícími prožitky kvůli obavám, že budou označeni za duševně nemocné. 49 O to důležitější roli sehrává lékař, který při vystavení receptu na kortikoidní medikaci informuje pacienta a jeho blízké o potenciálním riziku psychiatrických nežádoucích účinků. Časné poskytnutí informací o riziku manifestace psychiatrických komplikací v důsledku kortikoidní léčby a rovněž o možnosti zmírnění těchto obtíží může pacientovi pomoci překonat strach z duševního onemocnění a včas vyhledat potřebnou pomoc.
KRÁTKÉ KAZUISTIKY
11letá dívka po transplantaci plic pro obliterující bronchiolitidu psychiatricky vyšetřována v rámci rehospitalizace na pediatrii k došetření příčiny nárůstu tělesné hmotnosti s přibližně ročním odstupem od úspěšné transplantace. V době vyšetření medikována 10 mg prednisonu denně. Vyšetření pacientky žádáno pro zvýšenou dráždivost, plačtivost a podezření na depresivitu. V klinickém obraze zachycena zvýšená emoční labilita, sklon k impulzivitě s občasným auto agresivním chováním, dívka však připouští i suicidální ideace impulzivního charakteru, dosud bez tendencí k realizaci. Dále zachyceno i narušení spánku ve smyslu iniciální insomnie. Vzhledem k časové korelaci rozvoje obtíží se zahájením kortikoidní léčby po proběhlém operačním výkonu a zároveň relativní nepřítomnosti jiných významnějších faktorů vysvětlujících uvedené obtíže bylo vysloveno podezření na nežádoucí účinky kortikoidní medikace. Pacientce byl do medikace přidán quetiapin v dávce 25 mg na noc s možným navýšením dle stavu. Při kontrolním vyšetření s týdenním odstupem pacientka subjektivně referuje zlepšení stavu, ústup emoční lability a vymizení suicidálních ideací, rovněž pozorováno zlepšení spánku. Pacientka propuštěna na medikaci quetiapinem 25 mg do péče pedopsychiatrické ambulance.
9letá dívka s akutní lymfoblastickou leukémií hospitalizována na hematoonkologii během intenzivní fáze léčby leukémie. V průběhu onkologické léčby pacientka pro zvýšenou anxiozitu zamedikována sertralinem v dávce 50 mg. Opakovaně po zahájení kortikoterapie vysokými dávkami dexamethasonu u pacientky zaznamenáno náhlé zhoršení psychického stavu s nárůstem úzkosti, polymorfních bolestivých stesků, neztišitelný pláč a křik. Po vysazení kortikoidů vždy dochází k postupnému odeznění obtíží a normalizaci stavu. Ještě před pedopsychiatrickým vyšetřením do medikace přidán ošetřujícím lékařem bromazepam 1,5 mg 1krát denně ráno, vzhledem k přetrvávání obtíží vyžádáno psychiatrické konzilium. Pedopsychiatrem doporučeno vysazení bromazepamu, ponechán sertralin, do medikace přidán risperidon 2krát 0,25 mg a hydroxyzin 12,5 mg večer, doporučena podpůrná psychoterapeutická péče. Při kontrolním vyšetření s odstupem 3 dnů bylo patrno zlepšení stavu pacientky, obj. byla pacientka klidná, normoforická, bez tenze či anxiozity v dobrém kontaktu s personálem, plně spolupracující v rámci léčebného režimu. Po ukončení podávání vysokodávkovaného dexamethasonu postupně z medikace vysazen i risperidon, doporučeno ponechat pouze sertralin a hydroxyzin, opětovné zavedení risperidonu do medikace naplánováno před dalším podáváním kortikoidů, následně pacientka přeložena na krajské pracoviště s doporučením pokračovat v pedopsychiatrické konziliární péči.
ZÁVĚR
Přes obrovský terapeutický přínos v řadě somatických oborů medicíny jsou kortikoidy spojeny s řadou nežádoucích účinků. O těch psychiatrických bohužel stále víme poměrně málo. Zdrojem dat jsou zejména kazuistiky nebo studie malého rozsahu, chybějí nám přesnější vodítka ke zvládání jednotlivých typů komplikací a jejich profylaxi. Je třeba dalšího výzkumu k podrobnějšímu zmapování nežádoucích účinků a četnosti jejich výskytu při podávání jednotlivých kortikoidních preparátů, dále pak i k nalezení nejefektivnějších postupů při jejich léčbě. V rámci výzkumné práce je velmi důležitá přesná identifikace užívaných kortikoidů, jejich dávky, cesty podání a doby užívání do vzniku nežádoucích účinků, zejména však je nutný přesnější popis psychiatrických komplikací umožňující následnou psychiatrickou klasifikaci. V rámci běžné klinické praxe je pak nejdůležitější dostatečná informovanost lékařů a pacientů o potenciálním riziku vzniku nežádoucích účinků a o způsobech, jak lze danou situaci řešit.
LITERATURA
- 1. De Kloet ER, Joěls M, Holsboer F. Stress and the brain: From adaptation to disease. Nat Rev Neurosci 2005; 6 (6): 463-475.
- 2. McEwen BS. Stress and Hippocampal Plasticity. Annu Rev Neurosci 1999; 22 (1) : 105-122.
- 3. Woolley C, Gould E, McEwen B. Exposure to excess glucocorticoids alter dendritic morphology of adult hippocampal pyramidal neurons. Brain Res 1990; 531 (1-2): 225-231.
- 4. De Leon M, McRae T, Rusinek H et al. Cortisol reduces hippocampal glucose metabolism in normal elderly, but not in Alzheimer´s disease. J Clin Endocrinol Metab 1997; 82 (10): 3251-3259.
- 5. Hansson A, Cintra A, Belluardo N et al. Gluco- and mineralocorticoid receptor-mediated regulation of neurotrophic factor gene expression in the dorsal hippocampus and the neocor-tex of the rat. Eur J Neurosci 2000; 12 (8): 2918-2934.
- 6. Vellucci SV, Parrott RF, Mimmack ML. Down-regulation of BDNF mRNA, with no effect on trkB or glucocorticoid receptor mRNAs, in the porcine hippocampus after acute dexamethasone treatment. Res Vet Sci 2001; 70 (2): 157-162.
- 7. Duman RS, Monteggia LM. A Neu-rotrophic Model for Stress-Related Mood Disorders. Biol Psychiatry 2006; 59(12): 1116-1127.
- 8. Lupien SJ, De Leon M, De Santi S et al. Cortisol levels during human aging predict hippocampal atrophy and memory deficits. Nat Neurosci 1998; 1: 69-73.
- 9. De Quervain D, Henke K, Aerni A et al. Glucocorticoid-induced impairment of declarative memory retrieval is associated with reduced blood flow in the medial temporal lobe. Eur J Neurosci 2003; 17 (6): 1296-1302.
- 10. Mitchell C, Richards S, Kinsey S et al. Benefit of dexamethasone compared with prednisolone for childhood acute lymphoblastic leukaemia: Results of the UK Medical Research Council ALL97 randomized trial. Br J Haematol 2005; 129 (6): 734-745.
- 11. Bender B, Lerner J, Kollasch E. Mood and Memory Changes in Asthmatic Children Receiving Corticosteroids. J Am Acad Child Adolesc Psychiatry 1988; 27 (6): 720-725.
- 12. Upadhyay A, Mishra O, Prasad R, Upadhyay S, Schaefer F. Behavioural abnormalities in children with new-onset nephrotic syndrome receiving corticosteroid therapy: results of a prospective longitudinal study. Pediatr Nephrol 2015: 1-6.
- 13. Hall A, Thorley G, Houtman P. The effects of corticosteroids on behavior in children with nephrotic syndrome. Pediatr Nephrol 2003; 18 (12): 1220-1223.
- 14. Mrakotsky C, Forbes P, Bernstein J et al. Acute Cognitive and Behavioral Effects of Systemic Corticosteroids in Children Treated for Inflammatory Bowel Disease. J Int Neuropsychol Soc 2013; 19: 96-109.
- 15. Khan S, Hayat J, Raza S. Inhaled Steroid-Induced Mania in an Adolescent Girl. Prim Care Companion CNS Disord 2011; 13 (2): 13-15.
- 16. Morris D, Meighen K, McDougle G Acute Onset of Obsessive-Compulsive Disorder in an Adolescent With Acute Lymphoblastic Leukemia. Psychoso-matics 2005; 46 (5): 458-460.
- 17. Warrington T, Bostwick J. Psychiatric Adverse Effects of Corticosteroids. Mayo Clin Proc 2006; 81 (October): 1361-1367.
- 18. Lewis D, Smith R. Steroid-induced psychiatric syndromes. J Affect Disord 1983; 5 (4): 319-332.
- 19. Naber D, Sand P, Heigl B. Psycho-pathological and neuropsychological effects of 8-days´ corticosteroid treatment. A prospective study. Psychoneuroendocrinology 1996; 21 (1): 25-31.
- 20. Bolanos SH, Khan DA, Hanczyc M et al. Assessment of mood states in patients receiving long-term corticosteroid therapy and in controls with patient-rated and clinician-rated scales. Ann Allergy Asthma Immunol 2004; 92 (5): 500-505.
- 21. Bratek A, Kozmin-Burzynska A, Górniak E, Krysta K. Psychiatric Disorders Associated with Cushings Syndrome. In: Psychiatria Danubina. Vol 27.; 2015: 339-343.
- 22. Fardet L, Petersen I, Nazareth I. Suicidal Behavior and Severe Neuropsychiatric Disorders Following Glucocorticoid Therapy in Primary Care 2008; 17: 491-497.
- 23. Lupien SJ, McEwen BS. The acute effects of corticosteroids on cognition: Integration of animal and human model studies. Brain Res Rev 1997; 24 (1): 1-27.
- 24. Tavassoli N, Montastruc-Fournier J, Montastruc JL. Psychiatric adverse drug reactions to glucocorticoids in children and adolescents: A much higher risk with elevated doses. Br J Clin Pharmacol 2008; 66 (4): 566-567.
- 25. Sirois F. Steroid psychosis: A review. Gen Hosp Psychiatry 2003; 25 (1): 27-33.
- 26. Nishimura K, Harigai M, Omori M, Sato E, Hara M. Blood-brain barrier damage as a risk factor for corticosteroid-induced psychiatric disorders in systemic lupus erythematosus. Psychoneuroendocrinology 2008; 33 (3): 395-403.
- 27. Ling MH, Perry PJ, Tsuang MT. Side effects of corticosteroid therapy. Psychiatric aspects. Arch Gen Psychiatry 1981; 38 (4): 471-477.
- 28. Galen DM, Beck M, Buchbinder D. Steroid psychosis after orthognathic surgery: a case report. J Oral Maxillofac Surg 1997; 55 (3): 294-297.
- 29. Teuffel O, Kuster SP, Hunger SP. Dexamethasone versus prednisone for induction therapy in childhood acute lymphoblastic leukemia: A systematic review and meta-analysis. Leukemia 2011; 25 (8): 1232-1238.
- 30. Felder-Puig R, Scherzer C, Baumgartner M et al. Glucocorticoids in the treatment of children with acute lymphoblastic leukemia and Hodgkin´s disease: A pilot study on the adverse psychological reactions and possible associations with neurobiological, endocrine, and genetic markers. Clin Cancer Res 2007; 13 (23): 7093-7100.
- 31. Silverman M, Sheffer AL, Diaz PV, Lindberg B. Safety and tolerability of inhaled budesonide in children in the Steroid Treatment As Regular Therapy in early asthma (start) trial. Pediatr Allergy Immunol 2006; 17 (Suppl. 17): 14-20.
- 32. Greeves JA. Rapid-onset steroid psychosis with very low dosage of prednisolone. Lancet 1984: 1119-1120.
- 33. Campbell BA, Panicker J. New onset psychosis in an adolescent during treatment of testicular germ cell tumor. J Pediatr Hematol Oncol 2011; 33 (3): el25-el26.
- 34. Patten SB, Neutel CI. Corticosteroid-induced adverse psychiatric effects: incidence, diagnosis and management. Drug Saf 2000; 22 (2): 111-122.
- 35. Soliday E, Grey S, Lande MB. Behavioral effects of corticosteroids in steroid-sensitive nephrotic syndrome. Pediatrics 1999; 104 (4): e51.
- 36. Finkenbine R, Gille H. Case of Mania Due to Prednisone-Clarithromycin Interaction 1997; 42 (7): 778.
- 37. Finkenbine R, Frye M. Case of Psychosis due to Prednisone-Clarithromycin Interaction. Dent Traumatol 2005; 21: 344-346.
- 38. Judd LL, Schettler PJ, Brown ES et al. Adverse Consequences of Glucocorticoid Medication: Psychological, Cognitive, and Behavioral Effects. Am J Psychiatry 2014; (October): 1045-1051.
- 39. Brown ES. Effects of glucocorticoids on mood, memory, and the hippocampus: Treatment and preventive therapy. Ann NY Acad Sci 2009; 1179: 41-55.
- 40. Kenna HA, Poon AW, De Los Angeles CP, Koran LM. Psychiatrie complications of treatment with corticosteroids: Review with case report. Psychiatry Clin Neurosci 2011; 65 (6): 549-560.
- 41. Ularntinon S, Tzuang D, Dahl G, Shaw RJ. Concurrent Treatment of Steroid-Related Mood and Psychotic Symptoms With Risperidone. Pediatrics 2010; 125 (5): el241-el245.
- 42. Sherwood Brown E, Chamberlain W, Dhanani N et al. An open-label trial of olanzapine for corticosteroid-induced mood symptoms. J Affect Disord 2004; 83 (2-3): 277-281.
- 43. Kimmel RJ, Combs H. Steroid-Induced Mania Treated with Aripiprazole. Psychosomatics 2012; 53 (2): 181-183.
- 44. Falk WE, Mahnke MW, Poskanzer DC. Lithium Prophylaxis of Corticotropin-Induced Psychosis. JAMA 1979; 241 (10).
- 45. West S, Kenedi C. Strategies to prevent the neuropsychiatric side-effects of corticosteroids: a case report and review of the literature. Curr Opin Organ Transplant 2014; 19 (2): 201-208.
- 46. Brown ES, Wolfshohl J, Shad MU, Vazquez M, Osuji IJ. Attenuation of the effects of corticosteroids on declarative memory with lamotrigine. Neuropsychopharmacology 2008; 33 (10): 2376-2383.
- 47. Brown ES, Vazquez M, Nakamura A. Randomized, Placebo-Controlled, Crossover Trial of Memantine for Cognitive Changes with Corticosteroid Therapy. Biol Psychiatry 2008; 64 (8): 727-729.
- 48. McGrath P, Rawson-Huff N. Corticosteroids during continuation therapy for acute lymphoblastic leukemia: The psycho-social impact. Issues Compr Pediatr Nurs 2010; 33 (1): 5-19.
- 49. Reckart MD, Eisendrath SJ. Exogenous Corticosteroid Effects on Mood and Cognition: Case Presentations. Int JPsychosom 1990; 37 (1-4).





