Česká a slovenská psychiatrie

Časopis
Psychiatrické společnosti ČLS JEP
a Psychiatrickej spoločnosti SLS
souborný článek / review article
TRAZODON - FARMAKOLOGICKÝ PROFIL MULTIMODÁLNÍHO ANTIDEPRESIVA
TRAZODONE - PHARMACOLOGICAL PROFILE OF MULTIMODAL ANTIDEPRESSANT
Jan Juřica
Farmakologický ústav LF MU, Brno
SOUHRN
Juřica J. Trazodon - farmakologický profil multimodálního antidepresiva
Článek podává přehled molekulárních mechanismů působení trazodonu a odkrývá tak podstatu jeho antidepresivního účinku ve vyšším dávkování při zachování jeho dobré snášenlivosti a bezpečnosti. Důvodem zachování dobré snášenlivosti je dostupnost lékové formy s prodlouženým uvolňováním, která zabezpečí plošší farmakokinetickou křivku i při podání vyšší dávky, která je nutná pro inhibici serotoninového transportéru a antagonismus receptorů 5HT2A a 5HT2C.
V článku je také shrnuta farmakokinetika, bezpečnost, interakční potenciál trazodonu a jeho místo v klinické praxi.
Klíčová slova: trazodon, farmakologický profil, multimodální antidepresiva, bezpečnost
SUMMARY
Juřica J. Trazodone - pharmacological profile of multimodal antidepressant
The article reviews the molecular mechanisms of action of trazodone and thus reveals the basic principles of its antidepressant action at higher dosages while preserving its good tolerability and safety. This is due to the availability of sustained release dosage form that provides rather flat pharmacokinetic curve even at the higher doses required for serotonin transporter inhibition and 5HT2A and 5HT2C receptor antagonism. Finally, pharmacokinetics, safety, interaction potential of trazodone and its place in clinical practice are also summarized.
Key words: trazodone, pharmacological profile, multimodal antidepressants, safety
ÚVOD
Trazodon, triazolopyridinový derivát, byl syntetizován již v r. 1964, jako antidepresivum se začal používat o několik let později a teprve postupně se učíme, jak maximálně využít jeho terapeutický potenciál. Pokroky v maximalizaci využití trazodonu jsou založeny na postupném odkrývání a pochopení mechanismů jeho působení. Tyto mechanismy se zapojují do účinku v závislosti na podané dávce, respektive v závislosti na koncentraci tohoto léčiva v místě účinku. Trazodon je od r. 1996 obvykle řazen mezi tzv. SAKI antidepresiva - tedy inhibitory zpětného vychytávání serotoninu a antagonisty serotoninových receptorů. Dle nomenklatury NbN (Neuroscience-based Nomenclature) je však označován především jako antagonista 5HT2 receptorů a agonista 5HT1A receptorů - tyto aktivity dle NbN vstupují do popředí mechanismu jeho antidepresivního působení. Nutno přiznat, že tato klasifikace přesněji odráží selektivitu jeho působení v nízkých koncentracích. Je indikován k léčbě deprese různé etiologie, včetně deprese provázené úzkostí, poruchami spánku nebo sexuální dysfunkcí neorganického původu, kdy díky receptorovému profilu vystupují do popředí výhodné vlastnosti trazodonu. Off label se v některých zemích používá i v řadě jiných indikací, jako je např. posttraumatická stresová porucha, poruchy příjmu potravy, obsedantně-kompulzivní porucha, poruchy chování spojené s užitím látek (F10-F19), poruchy chování způsobené kognitivní poruchou, sexuální dysfunkce, a dokonce i jako doplňková léčba bolesti.1
RECEPTOROVÝ PROFIL, MULTIMODALITA ÚČINKU TRAZODONU
Jak již bylo uvedeno, receptorová afinita trazodonu je velmi závislá na koncentraci, resp. podané dávce. Trazodon vykazuje vícero mechanismů působení (multifunkční antidepresivum). Jedním z těchto mechanismů je antagonismus na receptorech, přičemž tento antagonismus je selektivní a na dávce/koncentraci závislý. V nejnižších koncentracích antagonizuje 5HT2A, ?1 a histaminergní H1 receptory. Především antagonismus H1 histaminergních receptorů pomáhá vysvětlit jeho hypnosedativní účinky při nejnižších dávkách okolo 50-75 mg/den.2,3 Trazodon dále vykazuje 5HT1A agonistické účinky, což se podařilo prokázat opakovaně v preklinických experimentech.4 Teprve při troj- až pětinásobném zvýšení koncentrace (odpovídá dávkám 200-600 mg/den) dochází k antagonismu na ? 2 receptorech, inhibici serotoninového transportéru, k blokádě 5HT2C receptorů a k plnému rozvinutí antidepresivní účinnosti.3,5,6 Schopnost antagonizovat 5HT2A receptory byla přesvědčivě dokumentována elektrofyziologickými studiemi - např. i s použitím selektivního agonisty receptorů 5HT2A (DOI, [1-(2,5-dimetoxy-4-jodofenyl-2-aminopropan hydrochlorid) ], jehož účinek dokázal trazodon zvrátit.6 Podobně je v animálních modelech dokumentován antagonismus 5HT2C receptorů.6,7 Dávková, resp. koncentrační selektivita se uplatňuje i v účinku mnoha dalších léčiv, mj. i quetiapinu, zde můžeme pozorovat jistou analogii (hypnotický účinek - antidepresivní účinek - antipsychotický účinek). Tento receptorový profil trazodonu je jak z pohledu účinnosti, tak z pohledu snášenlivosti velmi výhodný. Jednotlivé receptorové aktivity se zapojují v závislosti na koncentraci - nejnižší (hypnotické) dávky jsou schopné ze 100 % antagonizovat 5HT2A receptory (koncentrace cca 1Okrát Kd) a z více než 50 % antagonizují ?1 a H1 receptory - což je skutečně dostačující pro hypnotický účinek. Tyto dávky ovšem inhibují SERT jen asi z 50 %, přičemž pro antidepresivní účinek je třeba téměř kompletní blokáda SERT.3 Na rozdíl od poměrně neselektivního zvýšení koncentrací serotoninu, ke kterému dochází po silnější blokádě SERT při podání SSRI, však nedochází ke stimulaci všech serotoninergních receptorů (tedy i 5HT2A, 5HT2C, 5HT3), ale naopak při vyšších dávkách k jejich blokádě, a tak se neprojeví ani typické nežádoucí účinky SSRI, jako jsou zvracení, emoční oploštělost, petechie a sexuální dysfunkce.2,3,8 Sexuální dysfunkce jsou relativně častým nežádoucím účinkem SSRI nebo SNRI, který je připisován především neselektivnímu serotoninergnímu působení, které zahrnuje i aktivaci 5HT2A a 5HT2C receptorů. Teorie i klinické zkušenosti dokládají, že trazodon je v tomto ohledu selektivní a blokáda 5HT2A a HTT2C receptorů (pročež musí být ovšem podáván v patřičné dávce) těmto nežádoucím účinkům předchází. K objasnění této teorie může přispět i popis účinku flibanserinu - léčiva recentně registrovaného pro terapii sexuálních dysfunkcí, s mechanismem účinku na podkladu antagonismu 5HT2A, 5HT2B, 5HT2C receptorů, D4 receptorů a agonismem 5HT1A receptorů, popř. úspěšné terapeutické pokusy při sexuálních dysfunkcích s mirtazapinem (antagonista 5HT2, 5HT3 a ? 2) nebo cyproheptadinem (antagonista 5HT2A).9
Další rozdíl je ve slabší blokádě serotoninového transportéru (SERT), kdy na rozdíl od skupiny SSRI nejsou po trazodonu hlášeny nežádoucí účinky stran krvácení a petechií,8,10 které jsou důsledkem blokády SERT v trombocytech.
Receptorová afinita sama o sobě však nedokáže plně a komplexně vysvětlit vliv na aktivitu monoaminergních drah a profil účinků trazodonu. Důvodem jsou nejen interakce zprostředkované presynaptickými autoreceptory ale i reciproční funkční interakce mezi receptorovými systémy - tedy v jistém smyslu "cross-talk" mezi serotoninergními, adrenergními, GABA-ergními a dopaminergními neurony. Jejich vzájemné ovlivnění je založeno na přítomnosti heteroreceptorů na daném nervovém vlákně. V dalších oddílech bude nastíněn tento "cross-talk" mezi jednotlivými receptorovými systémy.
OVLIVNĚNÍ VÝDEJE DOPAMINU ANORADRENALINU PROSTŘEDNICTVÍM HETERORECEPTORŮ 5HT2A/C
Serotonin může prostřednictvím svých 5HT2A/C heteroreceptorů na GABA-ergních interneuronech a následně vlivem tonického inhibičního účinku GABA snižovat výdej dopaminu a noradrenalinu.3,11,12 Inverzní agonisté 5HT2C zvyšují výdej DA ve striatu a nucleus accumbens.13 Tento mechanismus ovlivnění výdeje DA (a patrně i NA) je podkladem některých nežádoucích účinků neselektivního působení SSRI, jako jsou snížení pozitivních i negativních emocí a celková emoční oploštělost nebo apatie.14 Antagonismus 5HT2A/C receptorů může být cenný u některých typů deprese, jak dokládá jeden z mechanismů účinků trazodonu i mirtazapinu nebo pokusy o augmentaci např. quetiapinem nebo jinými antipsychotiky.13,15
Preklinické práce dokazují, že trazodon zvyšuje noradrenergní transmisi po její inhibici selektivním 5HT2A agonistou (DOI, 1-(2, 5-dimetoxy-4-iodofenyl-2-amino-propan hydrochlorid)],6 a v sérii experimentů dokládají, že je to zprostředkováno právě antagonismem na 5HT2A receptorech. Podobně také noradrenalin prostřednictvím svých ?2 autoreceptorů snižuje výdej noradrenalinu,16 a tak ?2 antagonismus trazodonu může zvýšit jeho výdej.
INTERAKCE MEZI 5HT1A A VÝDEJEM DOPAMINU
Aktivace presynaptických 5HT1A receptorů vede ke snížení serotoninergní transmise, a nedochází tak k aktivaci postsynaptických 5HT2A receptorů. Tím dojde ke snížení aktivity GABA-ergních interneuronů a disinhibici výdeje dopaminu. Podobně i stimulace postsynaptických 5HT1A receptorů v kortexu vede ke snížení výdeje glutamátu, následně aktivity GABA-ergních interneuronů a následně k disinhibici výdeje dopaminu v kortexu.
Souhrnem lze konstatovat, že agonismus, resp. parciální agonismus presynaptických 5HT1A receptorů vede ke zvýšení výdeje dopaminu - v rafeálních jádrech středního mozku a v nigrostriatální dráze. Agonistickou, resp. parciálně agonistickou aktivitou 5HT1A je vysvětlována nižší schopnost působit extrapyramidové nežádoucí účinky u některých antipsychotik.16
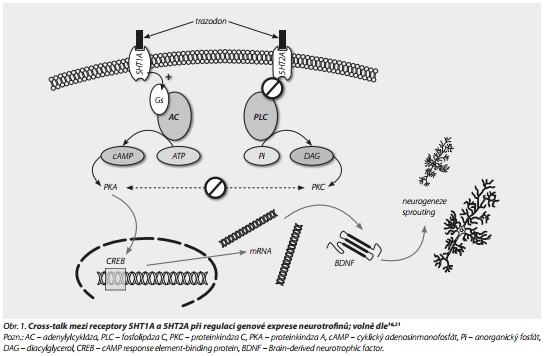
INTERAKCE MEZI 5HT1A, 5HT2A, 5HT2C A PRODUKCÍ BDNF
Neurotrofin BDNF (Brain Derived Neurotrophic Factor) hraje důležitou roli v neurogenezi a synaptické plasticitě.
Podporuje růst nervových vláken, jejich přežívání a synaptické rašení (sprouting).17 Zvýšení jeho exprese je považováno za jeden z mechanismů účinku antidepresiv a jeho podání má v experimentálních modelech účinky podobné antidepresivům.18 V mozcích pacientů s depresí byly post mortem nalezeny nižší hladiny BDNF.19 Je také známo, že serotonin dokáže na jedné straně zvýšit jeho produkci cestou aktivace 5HT1A receptorů (a následně proteinkinázy A) a na straně druhé snížit jeho produkci cestou aktivace receptorů 5HT2A (a následně fosfolipázy C),16 proto je i z tohoto pohledu výhodná schopnost trazodonu účinkovat jako parciální agonista 5HT1A a současně jako antagonista 5HT2A - tato interakce má synergický vliv na zvýšení exprese BDNF.16
Vedle této interakce mezi 5HT1A a 5HT2C receptory je možno hypotetizovat, že i antagonismus 5HT2C může dále zvyšovat expresi BDNF. Agonismus 5HT2C totiž aktivuje osu hypotalamus-hypofýza-nadledviny a zvyšuje tak hladiny glukokortikoidů.20 Také je známo, že při stresu dochází zvýšením produkce glukokortikoidů ke snížení BDNF v hipokampu.21 Antagonismus na 5HT2C by mohl tyto efekty zprostředkované glukokortikoidy mírnit, nebo přinejmenším nezhoršovat.
HYPNOTICKÝ ÚČINEK
K hypnotickému účinku přispívá blokáda 5HT2A receptorů, ke které dochází již při dávkách okolo 10 mg, ovšem plný hypnotický účinek se rozvine až při blokádě ?1 a H1 receptorů, a to až při dávkách 25-100 mg. Dokladem toho, že 5HT2A potencuje hypnotický účinek, je eplivanserin - jedná se o antagonistu 5HT2A receptorů, léčivo, které bylo vyvíjeno jako nové hypnotikům, ovšem jeho vývoj byl v r. 2009 pozastaven.
Antagonismus 5HT2A a H1 receptorů je s ohledem na hypnotický účinek posílen i antagonismem ?1 receptorů.2 Vedle zmíněných mechanismů může trazodon interferovat se sekrecí melatoninu, jehož noční sekreci zvyšuje, během dne však nemění.22
ANXIOLYTICKÝ ÚČINEK
Přestože trazodon není indikován k léčbě úzkostných poruch, vykazuje anxiolytické působení, které je dané především jeho 5HT1A agonistickým a snad i ?2 antagonistickým působením.3,23 Aktivaci 5HT1A a anxiolytickému účinku odpovídá dávka okolo 150 mg denně. Pokud je dávka ještě vyšší (okolo 300 mg denně), dostaví se i blokáda 5HT2A a 2C receptorů, což může anxiolytický účinek ještě posílit. Agonismus 5HT1A a zároveň antagonismus 5HT2C totiž snižuje projevy strachu/úzkosti v preklinickém modelu24 a nakonec i účinek buspironu je založen především na 5HT1A parciálně agonistickém působení.
ANTIDEPRESIVNÍ ÚČINEK
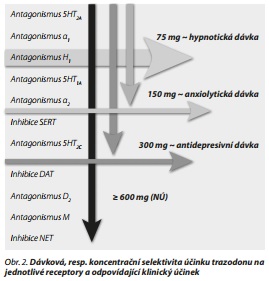
Antidepresivní účinek trazodonu je dobře prověřen a byl srovnatelný s účinkem TCA, SSRI i SNRI.2 Dostavuje se ovšem až při vyšších dávkách, než jaké byli doposud psychiatři zvyklí používat. Lepší toleranci těchto vyšších dávek umožnila především nová léková forma s modifikovaným uvolňováním, které zabezpečí vyrovnanější hladiny s plošší koncentrační křivkou. Mechanismem antidepresivního účinku je inhibice zpětného vychytávání serotoninu, agonistická, resp. parciálně agonistická aktivita na 5HT1A receptorech, desenzitizace rafeálních 5HT1A receptorů25 a v konečném důsledku díky posílení dopaminergní transmise (a také přinejmenším nepotlačení noradrenergní) i antagonismus 5HT2A a 5HT2C i ?1 receptorů.
MULTIFUNKČNOST A MULTIMODALITA
O trazodonu můžeme říci, že je zároveň multimodálním i multifunkčním léčivem a dle nové nomenklatury NbN, kterou se snaží prosadit do praxe všechny světové odborné společnosti, bývá označován jako serotoninové multimodální antidepresivum.26,27 Multifunkční antidepresiva popisuje Stahl jako léčiva s vícero mechanismy působení - tedy např. inhibice zpětného vychytávání noradrenalinu a inhibice zpětného vychytávání serotoninu. Vedle toho je i multimodální - např. inhibice zpětného vychytávání a zároveň receptorový antagonismus. V praxi tedy máme jak léčiva multifunkční s jedním "módem" působení (SNRI, agomelatin), tak i multifunkční a zároveň multimodální (např. vortioxetin nebo právě trazodon - inhibice SERT + antagonismus na ? 1; ?1; H1; HT2A a 5HT2C receptorech). Můžeme se ptát, zda vlastně většina antidepresiv není multimodálních nebo "alespoň" multifunkčních - zvláště při vyšších dávkách. Více mechanismů účinku, které ovšem vedou spíše k nežádoucím projevům (např. inhibice DAT a SERT + antagonismus na M receptorech), stěží označíme jako "multifunkční", spíše bývají označována jako "špinavá" léčiva. Multifunkční mechanismy jsou spíše ty, které se projeví při běžných terapeutických dávkách žádoucím (antidepresivním, anxiolytickým, antipsychotickým) účinkem - např. inhibice SERT + antagonismus 5HT2A, 5HT2C.26 Díky svému receptorovému profilu je trazodon svým způsobem flexibilní a může být použit s výhodou u několika komorbidit deprese.
FARMAKOKINETIKA
Farmakokinetika trazodonu je definována především vlastnostmi lékové formy. Žádné lékové formy s trazodonem s kinetikou absorpce 1. řádu (tablety bez modifikovaného uvolňování, kapky) nejsou v České republice na trhu.
Po podání tablet s řízeným uvolňováním (Trittico AC) dochází k prodloužené fázi absorpce s maximální koncentrací v plazmě za 4 hodiny (= Tmax) a eliminačním poločasem okolo 12 hodin. Po podání vyšších dávek v lékové formě s prodlouženým uvolňováním (Trittico Prolong) se prodlouží Tmax na 6-8 hodin a se zvyšující se dávkou v rozmezí od 75 do 375 mg roste lineárně maximální koncentrace v plazmě (Cmax) i plocha pod koncentrační křivkou (AUC). Eliminační poločas je pak asi 13 hodin. Steady state je po opakovaném podání dosaženo po 5 dnech podávání. Zajímavá je chronofarmakokinetika trazodonu - po podání večer jsou Cmax cca o 50 % vyšší než při podání ráno, nicméně AUC jsou srovnatelné. Jídlo, zvláště tučné, zvyšuje Cmax, ovšem neovlivňuje Tmax. Mihara et al. uvádějí, že plazmatická hladina trazodonu, která postačuje pro dobrý terapeutický účinek, je asi 700 ng/mL.28 Trazodon podléhá rozsáhlé jaterní biotransformaci cytochromy P450 1A2, 3A4 a 2D6. Hlavním metabolitem je m-chloro-fenylpiperazin (mCPP), kterýje spíše anxiogenní a působí jako agonista na receptory 5HT2A i 5HT2C (vedle toho i na 5HT1A, 5HT1D). Tento metabolit je ovšem v mozku v koncentraci odpovídající asi 10 % koncentrace trazodonu, a tak při kompetici s ním výše uvedené receptory prakticky neovlivňuje.28
BEZPEČNOST, INTERAKČNÍ POTENCIÁL
Trazodon je obecně velmi dobře tolerován, typickými nežádoucími účinky jsou ospalost (přechodně), bolest hlavy, sucho v ústech. Přestože trazodon nepůsobí anticholinergně, může způsobit prodloužení QT intervalu, ovšem v ohledu proarytmogenního účinku je celkově vzato bezpečnější než TCA. U pacientů s preexistujícím onemocněním srdce může být proarytmogenní.10,29
U starších osob by mohl trazodon s ohledem na jeho antagonismus ?1 receptorů způsobit ortostatickou hypotenzi - tento nežádoucí účinek je přechodný a závislý na plazmatické koncentraci.2 Podobně jsou starší pacienti citlivější k ospalosti, popř. zácpě.29
Trazodon je metabolizován enzymem CYP3A4, ale neinhibuje jej. Z toho vyplývá, že plazmatické koncentrace trazodonu mohou být při kombinaci s inhibitory CYP3A4 (např. azolová antimykotika, erytromycin, antiretrovirotika) zvýšeny a také může být vyšší četnost nežádoucích účinků. Na druhé straně koncentrace, a tím i účinnost, může být snížena při kombinaci s induktory CYP3A4, jako je např. karbamazepin, modafinil, glukokortikoidy nebo rifampicin. Ve spektru farmakodynamických interakcí je třeba myslet na aditivní sedativní a proarytmogenní účinek a nekombinovat trazodon s TCA, alkoholem nebo s ohledem na teoretické riziko serotoninového syndromu s TCA, iMAO nebo fluoxetinem. Na druhou stranu bylo také publikováno, že kombinace s některými SSRI (citalopram, fluoxetin) je z pohledu serotoninového syndromu bezpečná.30 Při poškození renálních funkcí není třeba úpravy dávky, zatímco u těžkého jaterního poškození nebo ikteru se trazodon podávat vůbec nemá.
ZÁVĚR
Trazodon je cenným léčivem v armamentáriu psychiatrů. Je přínosný především pro depresivní pacienty, kteří trpí nespavostí, bojí se váhového přírůstku, popř. se obávají sexuálních nežádoucích účinků antidepresivní terapie. V některých metaanalýzách účinnosti byl neprávem opomenut; doklady o jeho klinické účinnosti jsou vcelku přesvědčivé. S lékovou formou s vyšší dávkou a prodlouženým uvolňováním má potenciál být prospěšný pro širší spektrum pacientů a může překonat farmakoterapeutickou "pseudorezistenci" způsobenou příliš nízkou dávkou trazodonu. Vzhledem k tomu, že neinhibuje zásadně biotransformační cesty jiných léčiv, může být pro polymorbidní pacienty alternativou k jiným antidepresivům inhibujícím enzymy cytochromu P450.
LITERATURA
- 1. Khouzam HR. A review of trazodone use in psychiatrie and medical conditions. Postgrad Med. Jan 2017; 129 (1): 140-148.
- 2. Fagiolini A, Comandini A, Catena Dell´Osso M, Kasper S. Rediscovering trazodone for the treatment of major depressive disorder. CNS Drugs. Dec 2012; 26 (12): 1033-1049.
- 3. Stahl SM. Mechanism of action of trazodone: a multifunctional drug. CNS Spectr. Oct 2009; 14 (10): 536-546.
- 4. Odagaki Y, Toyoshima R, Yamauchi T. Trazodone and its active metabolite m-chlorophenylpiperazine as partial agonists at 5-HT1A receptors assessed by [35S]GTPgammaS binding. J Psychopharmacol. May 2005; 19 (3): 235-241.
- 5. Čéšková E. Trazodon v léčbě insomnie. Practicus. 2013; 12 (4): 17-19.
- 6. Ghanbari R, El Mansari M, Blier P. Electrophysiological impact of trazodone on the dopamine and norepinephrine systems in the rat brain. Eur Neuropsychopharmacol. Jul 2012; 22 (7): 518-526.
- 7. Balsara JJ, Jadhav SA, Gaonkar RK, Gaikwad RV, Jadhav JH. Effects of the antidepressant trazodone, a 5-HT 2 A/2C receptor antagonist, on dopamine-dependent behaviors in rats. Psychopharmacology (Berl). May 2005; 179 (3): 597-605.
- 8. Dynamed. EBSCO Information Services. 1995-2017; 2017. Updated Last Updated Date.
- 9. Rizvi SJ, Kennedy SH. Management strategies for SSRI-induced sexual dysfunction. J Psychiatry Neurosci. Sep 2013; 38 (5): E27-28.
- 10. InfoPharm. AISLP; 2017.
- 11. Di Giovanni G, De Deurwaerdére P, Di Mascio M, Di Matteo V, Esposito E, Spampinato U. Selective blockade of serotonin-2C/2 B receptors enhances mesolimbic and mesostriatal dopaminergic function: a combined in vivo electrophysiological and microdialysis study. Neuroscience. 1999; 91 (2): 587-597.
- 12. Millan MJ, Dekeyne A, Gobert A. Serotonin (5-HT)2C receptors tonically inhibit dopamine (DA) and noradrenaline (NA), but not 5-HT, release in the frontal cortex in vivo. Neuropharmacology Jul 1998; 37 (7): 953-955.
- 13. Chagraoui A, Thibaut F, Skiba M, Thuillez C, Bourin M. 5-HT2C receptors in psychiatric disorders: A review. Progress in Neuro-Psychopharmacology & Biological Psychiatry. Apr 32016; 66: 120-135.
- 14. Price J, Cole V, Goodwin GM. Emotional side-effects of selective serotonin reuptake inhibitors: qualitative study. Br J Psychiatry. Sep 2009; 195 (3): 211-217.
- 15. Hoschl C. Serotoninergní mechanismy účinku multifunkčních antidepresiv a některých antipsychotik. Psychiatrie. 2015; 19 (1): 44-48.
- 16. Stahl SM. Stahl´s Essential Psychopharmacology Cambridge University Press; 2013.
- 17. Homberg JR, Molteni R, Calabrese F, Riva MA. Tne serotonin-BDNF duo: developmental implications for the vulnerability to psychopathology. Neurosci Biobehav Rev. Jun 2014; 43: 35-47.
- 18. Zhou C, Zhong J, Zou B, et al. Meta-analyses of comparative efficacy of antidepressant medications on peripheral BDNF concentration in patients with depression. PLoS One. 2017; 12 (2): e0172270.
- 19. Chen B, Dowlatshahi D, MacQueen GM, Wang JF, Young LT Increased hippocampal BDNF immunoreactivity in subjects treated with antidepressant medication. Biol Psychiatry. Aug2001; 50 (4): 260-265.
- 20. Heisler LK, Pronchuk N, Nonogaki K, et al. Serotonin activates the hypothalamic-pituitary-adrenal axis via serotonin 2C receptor stimulation. J Neurosci. Jun 2007; 27 (26): 6956-6964.
- 21. Schaaf MJ, Sibug RM, Duurland R, et al. Corticosterone effects on BDNF mRNA expression in the rat hippocampus during morris water maze training. Stress. Dec 1999; 3 (2): 173-183.
- 22. Giannaccini G, Masala I, Palego L, et al. Melatonin and pro-hypnotic effectiveness of the antidepressant Trazodone: A preliminary evaluation in insomniac mood-disorder patients. Clinical Biochemistry. OCT 20162016; 49 (15) : 1152-1158.
- 23. Blier P, Ward NM. Is there a role for 5-HT1A agonists in the treatment of depression? Biol Psychiatry. Feb 2003; 53 (3): 193-203.
- 24. de Paula B, Leite-Panissi C. Distinct effect of 5-HT1A and 5-HT2A receptors in the medial nucleus of the amygdala on tonic immobility behavior. Brain Research. JUL 1520162016; 1643: 152-158.
- 25. Celada P, Puig M, Amargós-Bosch M, : Adell A, Artigas F. The therapeutic role of 5-HT1A and 5-HT2A receptors in depression. J Psychiatry Neurosci. Jul 2004; 29 (4): 252-265.
- 26. Stahl SM. Multifunctional drugs: a novel concept for psychopharmacology. CNS Spectr. Feb 2009; 14 (2): 71-73.
- 27. Nutt D. Beyond psychoanaleptics - can we improve antidepressant drug nomenclature? Journal of Psychopharmacology. JUN 20092009; 23 (4): 343-345.
- 28. Mihara K, Yasui-Furukori N, Kondo T, et al. Relationship between plasma concentrations of trazodone and its active metabolite, m-chlorophenyl-piperazine, and its clinical effect in depressed patients. Ther Drug Monit. Aug 2002; 24 (4): 563-566.
- 29. Lyseng-Williamson KA. Trazodone prolonged release: a guide to its use in depression. Drugs & Therapy Perspectives. 2015; 31: 137-142.
- 30. Prapotnik M, Waschgler R, Kónig P, Moll W, Conca A. Therapeutic drug monitoring of trazodone: are there pharmacokinetic interactions involving citalopram and fluoxetine? Int J Clin Pharmacol Ther. Feb 2004; 42 (2): 120-124.





